Реакция - диборан
Cтраница 3
На рис. 7 покапан ЯМР-спектр бора-11 в продукте реакции диборана с триметиламином. [31]
Как уже было сказано во введении к данной главе, реакции диборана с замещенными циклоолефинами протекают с цис-присоединением В - Н к двойной связи олефина. Так, из диборана и 1-метилциклопентена, 1-метилциклогексена и 1-фенил-циклогексена [165] были соответственно получены, после окисления, транс - 2-метилциклопентанол, транс - 2-метил - и транс - 2-фенилциклогексанолы. [32]
В качестве другого примера приведем Диспропорционирование смешанных алкилборов, образующихся при реакции диборана и олефина. Известно также, что многие алкилборгидриды при комнатной или более низкой температуре легко диспропор-ционируют, давая гидрид бора и алкильные производные бора. [33]
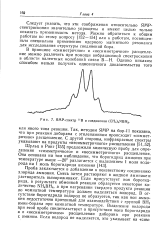 |
ЯМР-спектр В в соединении ( CH3 3NBH3. [34] |
Так, методом ЯМР на бор - И показано, что при реакции диборана с этиленамином происходит симметричное расщепление. [35]
Таким образом, как Шток, так и все другие исследователи, принимавшие продукты реакции диборана с водными растворами едкого кали за гипоборат калия или оксипроизводные борогидрида калия, имели в действительности дело со смесями бората калия КВ ( ОН) 4 и борогидрида калия КВН4 в различных соотношениях. [36]
Шлезингер и Берг [188] в обзорной статье кратко сообщили об образовании твердого аддукта Н3В - NCCH3 при реакции диборана с ацетонитрилом, диссоциирующего при комнатной температуре и частично превращающегося при этом в нелетучую жидкость. [37]
Больший выход 1 2-диарилдиборанов из эфиров диарилборных кислот объясняется тем, что при этой реакции возникает в 4 раза меньше эфира борной кислоты, чем в реакции диборана с эфирами арилборных кислот. [38]
Разрыв связей N - Р и Р - Р в первых трех случаях, по-видимому, был вызван побочными продуктами, что можно иллюстрировать более наглядно реакциями диборана с N - Р - и Р - Р - со-единениями. Правда, гидрид из группы борина здесь играет другую роль и не является агентом для восстановления связи между неметаллическими атомами. [39]
Приведенные выше методы гидратации по правилу Марковни-кова дополняются близким и эффективным методом гидроборирова-ния-окисления с обратной региоселективностью. Реакция диборана с затрудненными алкеном, подобным а-пинену, может протекать только до моно - или диалкилборана, который затем используется в качестве менее реакционноспособного и более селективного гидро-борирующего агента. [40]
Получение из диборана и спиртов. Реакция диборана со спиртами, приводящая при избытке последних к боратам, может быть использована для получения промежуточных продуктов алкоголиза - диалкокси-боранов, если реагенты брать в соответствующем стехиометрическом соотношении. [41]
Приведенные выше методы гидратации по правилу Марковни-кова дополняются близким и эффективным методом. Реакция диборана с затрудненными алкеном, подобным а-пинену, может протекать только до моно - или диалкилборана, который затем используется в качестве менее реакционноспособного и более селективного гидро-борирующего агента. [42]
Стоун и сотрудники нашли, что полученный твердый продукт содержит полимерный тетрафторэтилен, а также водород и бор. Летучие продукты реакций диборана с CF2 CF2, CF2CHF, CF2CH2 или CH2CHF представляли собой смесь олефинов, в которых фтор частично был замещен водородом. Бор в продуктах реакции содержался преимущественно в форме BF3, C2H5BF2, ( C2H) 2BF и ( C2Hs) sB, соединения же бора, содержащие фторэтильные радикалы, обнаружены не были. Для объяснения образования некоторых из этих продуктов было выдвинуто предположение, что первоначально происходит присоединение диборана к исходному олефину с последующим образованием связи бор - фтор посредством перехода фтора к бору 138 и сложность продуктов реакции обусловлена разнообразием возможностей присоединения промежуточно образующихся боринов к олефинам, присутствующим в реакционной смеси. [43]
Было найдено, что тетрафторэти-лен медленно реагирует с дибораном при комнатной температуре и быстро при 80, причем образуются этилбордифторид, диэтилборфторид и полимерный продукт. Также сложно протекают реакции диборана с трифторэтиленом, 1 1-дифторэтиленом и винилфторидом [ 91, в результате которых получаются продукты замещения фтора на водород, а также этилборфториды. [44]
Таким образом, избыток соединения, являющегося источником гидридного водорода - NaH, - способствует образованию более чистого конечного продукта - борогидрида натрия. В случае же реакции диборана с метилатом натрия по уравнению ( I), наоборот, увеличение концентрации диборана - также источника гидридного водорода - приводит к появлению метоксильных производных бора. [45]
Страницы: 1 2 3 4