Реакция - ионизация
Cтраница 1
Реакция ионизации и образования адсорбированного водорода является обратимой, и гистерезис кривой заряжения не наблюдается, если не заходить в область адсорбции кислорода. В области адсорбции водорода ( а и ж на кривых заряжения имеется перегиб, который указывает на существование двух форм адсорбированного водорода. [1]
Реакция ионизации 2 - ( и-метоксифенил) - 2-метилпропил-п - толуолсуль-фоната столь отчетливо определяется акцепторной силой растворителя, что логарифм константы скорости реакции можно использовать для описания кислотной силы этого растворителя [63] ( схему реакции см. на стр. Скорость реакции определяется силой сольватации толуолсульфонатного аниона OTs - - в переходном комплексе. [2]
Реакция ионизации характеризуется величиной степени ионизации, понятие о которой вводится аналогично понятию степени диссоциации для реакции диссоциации. [3]
Реакции ионизации описываются ур-ниями вида Ай А. Ап г Ап - р е; А0 обозначает нейтральный атом, Ап - л-кратно ионизованный атом, е - - электрон. [4]
Реакция ионизации молекулярного водорода может идти, минуя адсорбционную стадию, вне электрода, в непосредственной близости к поверхности. [5]
Реакция ионизации слабых кислот, т.е. их протолитическая реакция с слабоосновными растворителями, в частности с водой, приводит, как уже отмечалось в томе I, к равновесию, поддающемуся особенно точному измерению. Константа равновесия некоторой кислоты, называемая константой кислотности Ка, является мерой силы кислоты; говорят, что кислота сильная или слабая в зависимости от того, является ли ее константа большой или малой. [6]
Реакциям ионизации и рекомбинации ионов соответствуют вертикальные и горизонтальные переходы между соседними точками пространства конфигураций. Реакциям возбуждения и тушения уровней ионов - строго диагональные переходы, сохраняющие число электронов в конфигурации. [7]
Исследована реакция ионизации кислорода на серебряном и никелевом электродах, а также на композициях никель - серебро в растворах щелочи и влияние на эту реакцию различных форм электрохимически адсорбированного кислорода. [8]
Однако реакция ионизации карбоксильной группы идет быстрее, чем реакция связывания протонов, благодаря чему и происходит восстановление изоионного состояния. Таким образом, относительно более быстрое связывание анионов белком при соответствующем замедлении связывания протонов и являются причиной повышения изоионной точки белка в присутствии солей. Показано, например, что изоионная точка серу-мальбумина в присутствии 0 15 М хлористого натрия повышалась от рН 4 8 - 4 9 до 4 27, причем это изменение возрастало с увеличением концентрации белка. [9]
Равновесие реакций ионизации может быть смещено введением в пламя элемента с низким потенциалом ионизации. Для этой цели, как правило, используют соли калия или цезия. [10]
Потенциал реакции ионизации железа во всем интервале изменений рН остается на 50 мв отрицательнее равновесного водородного электрода, рассчитанного для Р н, 1 атм. [11]
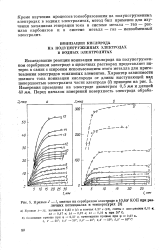 |
Кривые / - /, снятые на серебряном электроде в 10 6jV КОН при различных потенциалах и температурах. [12] |
Исследование реакции ионизации кислорода на полупогруженном серебряном электроде в щелочных растворах представляет интерес в связи с широким использованием этого металла для приготовления электродов топливных элементов. Измерения проведены на электроде диаметром 0 5 мм и длиной 40 мм. [13]
Осуществление реакции ионизации кислорода может привести также к синтезу молекул перекиси водорода. [14]
Изучение реакции ионизации кислорода на серебре и никеле, как и вообще на электродах из твердых металлов, представляет трудность вследствие неоднородной поверхности твердых электродов. Для реакции ионизации кислорода на серебре и никеле, как и для многих твердых электродов, характерным является то, что ионизация кислорода происходит в области потенциалов, при которых имеет место значительная адсорбция кислорода. [15]
Страницы: 1 2 3 4