Реакция - карбанион
Cтраница 1
Реакции карбанионов с карбонильными соединениями приводят к аддуктам, которые могут быть выделены в виде смеси двух диастереомеров, находящихся в равновесии друг с другом и с исходными соединениями. Они могут быть зафиксированы и разделены на соответствующие гидроксиалкилфосфиноксиды после протонирования. [1]
Реакции карбанионов с карбонильными соединениями приводят к аддуктам, которые могут быть выделены в виде смеси двух диастереомеров, находящихся в равновесии друг с другом и с исходными соединениями. Они могут быть зафиксированы и разделены на соответствующие гидроксиалкилфосфинокеиды после протонирования. [2]
О реакциях карбанионов, которые получаются из С - Н - кис-лотных соединений ( кетонов, сложных эфиров и др.), речь пойдет в разд. [3]
Обсуждаемые в этой главе реакции карбанионов мало отличаются от описанных в предыдущей. [4]
Реакции литийалкилов в общем рассматривают как реакции соответствующих карбанионов. Литийалкилы широко применяют как стереоспецифические катализаторы для полимеризации алке-нов, а именно изопрена, который при этом на 90 % превращается в 1 4 - г с-полиизопрен. Изучены и многочисленные другие реакции с алкенами. Комплексы литийалкилов с ТМЭДА особенно активны. Они не только полимеризуют этилен, но даже металлируют бензол и ароматические соединения, а также реагируют с водородом при 1 атм с образованием алкана и гидрида лития. [5]
Первые данные о возможности стереоспецифического образования и реакций карбанионов появились в 1955 г. [5]; с тех пор накопилось немало таких фактов и предложена теория, объясняющая эти результаты. [6]
 |
Стереохимия реакции расщепления карбанионов. [7] |
Со стереохимической точки зрения представляет интерес, что реакции карбанионов напоминают реакции ионов карбония ( ср. [8]
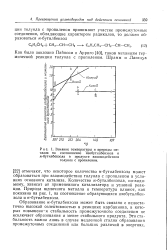 |
Влияние температуры и природы металла на соотношение изобутилбензола и н-бутилбензола в продукте взаимодействия толуола с пропиленом. [9] |
Образование н-бутилбензола может быть связано с недостаточно высокой селективностью в реакциях карбаниона, в которых повышенная стабильность промежуточного соединения не исключает образования и менее стабильного продукта. Эта стабильность важна лишь в случае медленной стадии образования промежуточных соединений или больших различий в энергиях. [10]
Катализируемое основаниями внутреннее алкилирование диенов и триенов с большими кольцами происходит вследствие реакции аллиль-ного карбаниона с двойной связью, как было описано выше для алки-лировация боковых цепей ароматических соединений ( разд. [11]
В уравнениях 27, 28 [28], 29 [13], 30 приведены примеры реакций карбанионов, стабилизированных сульфонимидоильной группой, с электрофильными реагентами. [12]
Реакция алкилирования удобна и отличается хорошими степенями конверсии, однако ей присущи все характерные для реакций карбанионов ограничения. Так, разветвление цепи у а-углеродного атома в заместителе RF, по-видимому, неизбежно, за исключением реакций с олефинами, содержащими только два атома углерода, поскольку карбанион получается в результате атаки фторид-иона на концевую CF2 - rpynny олефина и, следовательно, образования первичного перфторкабаниона не наблюдается в том случае, когда в цепи олефина содержится более двух атомов углерода. Кроме того, образование фторкарбанионов из перфтор-а-оле-финов осложняется протеканием обычно преобладающей конкурирующей реакции миграции двойной связи, которая приводит к образованию значительно менее реакционноспособного олефина с внутренней двойной связью. Например, реакция перфторбутадиена-1 3 с иианурфторидом вызывает лишь образование продукта с тройной связью ( СН3 - СС - CF3) и никакого алкилирования не происходит. [13]
Большинство критериев, разработанных для идентификации механизма полимеризации, относится к углеродным свободно-радикальным системам, к реакциям карбаниона или карбониевого иона. Если система содержит другие элементы, то эти критерии следует рассматривать только как ориентировочные. [14]
Нами разработаны теоретические основы применения метода нуклеофильного ароматического замещения водорода для синтеза азотсодержащих гетероциклических структур на основе реакции карбанионов арилацетонитрилов с нитроаренами и другими активированными системами. [15]
Страницы: 1 2 3