Реакция - обмен - водород
Cтраница 1
Реакция обмена водорода, присоединенного к бору в N-замещенных боразинах, в других отношениях детально не была исследована. Так как В-тригало-генборазины - намного более легко доступные соединения, их используют главным образом для последующих реакций обмена, поэтому отсутствие попыток осуществить обмен связанного с бором водорода вполне понятно. [1]
Реакция обмена водорода с дейтерием между 140 и 491 К: Н2 - f - D2 2HD, которая подробнее будет описана в следующей главе, при более высоких температурах происходит с преобладанием хемосорбции водорода. При низких температурах Смит и Тэйлор [54] обнаружили преимущественно физическую адсорбцию дейтерия. [2]
При реакции обмена водорода на дейтерий эти же окислы металлов на носителе, восстановленные при 500, становятся более активными. Так, данные табл. 6 указывают на увеличение скорости реакции каталитического обмена водород - дейтерий на окисных катализаторах после восстановления их водородом. [3]
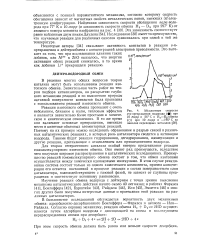 |
Абсолютные скорости о-я-превращения водорода ( при 10 торр и 26 С и Н3 - О2 - обмена ( О при 10 торр и - 196 С на окислах переходных металлов. [4] |
Изучение реакции обмена водорода с дейтерием с точки зрения выяснения механизма каталитического действия начато около 40 лет назад; в работах Фаркаса [41], Бонгоффера [42], Бурштейн [43], Райдила [44], Или [45], Эмметта [46] и многих других были получены интересные данные о протекании этой реакции на различных катализаторах. [5]
Активность в реакции обмена водорода на дейтерий наблюдается только для катализаторов, имеющих как электронодонорные, так и электроно-акцепторные свойства и практически отсутствует у алюмосиликатов, которые обладают незначительной восстановительной силой. Тем не менее, полученные данные содержат мало доказательств в пользу того, что окислительно-восстановительная активность является решающим фактором для процесса обмена, поскольку активность в передаче электрона у окиси алюминия все еще быстро возрастает для температур активации 550 - 650 С, тогда как активность в реакции обмена быстро уменьшается. [6]
Ацилированием называется реакция обмена водорода аминогруппы, оксигруппы или ароматического кольца на ацильную группу ( ацил) - остаток карбоновой или кислородсодержащей минеральной кислоты. [7]
Пиридин вступает в реакцию обмена водорода с гораздо большей скоростью, чем бензол. Это объясняется наличием в кольце электроотрицательного атома азота. По кинетической СН-кислотности пиридин похож на фторбеизол, однако между ними имеется одно важное различие. В молекуле фторбеизола более кислой является ближайшая к атому фтора связь СН в положении 2 и кислотность уменьшается в последовательности 2 - СН3 - СН4 - СН. [8]
Водород является ядом для реакции обмена водорода с дейтерием. Обмен протекает при температурах, при которых дейтерий не обменивается с водородом, удерживаемым катализатором. Источником каталитической активности является не недостаток кислорода на поверхности, а возникающая при дегидратации деформированная поверхность, обладающая повышенной энергией. [9]
Коури и Уэст [52] изучали реакцию обмена водорода на галоид в системе силан - трифенилгалоидметан и показали, что реакция идет в таких лолярных растворителях, в которых ( Происходит диссоциация связи С-Hai ( нитрометан, нитробензол, дихлорэтан) и не идет в неполярных растворителях, в которых не наблюдается диссоциация. Дифенилгалоидметан и третичный бутилхлорид не взаимодействуют с силаном. [10]
В дальнейшем гидроксид вступает в реакцию обмена водорода органической кислоты RCOOH на металл с образованием солей и воды: М ( ОН) 2 2 RCOOH - ( RCOO) 2 М 2Н2 О, где М - металл. [11]
Ввиду того что алкоголяты металлов претерпевают быстропротекающие реакции обмена водорода и металла, в качестве источника водорода можно использовать спирт в присутствии лишь каталитического количества алко-голята алюминия. Наиболее часто применяют изопропиловьга спирт и изо-пропилат алюминия. Реакции можно довести до высокой стецени превращения, непрерывно удаляя ацетон посредством перегонки. [12]
Ввиду того что алкоголяты металлов претерпевают быстропротекающие реакции обмена водорода и металла, в качестве источника водорода можно использовать спирт в присутствии лишь каталитического количества алко-голята алюминия. Наиболее часто применяют изопропиловый спирт и изо-пропилат алюминия. Реакции можно довести до высокой степени превращения, непрерывно удаляя ацетон посредством перегонки. [13]
При обработке кислотами ароматические соединения вступают в реакции обмена водорода. [14]
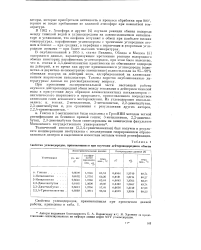 |
Свойства углеводородов, применявшихся при изучений дейтероводородного обмена. [15] |
Страницы: 1 2 3 4