Реакция - окисление - азот
Cтраница 2
Вывод уравнений зависимости lg Kpf ( Т) для реакций окисления азота осуществим сначала приближенным методом автора. Для этого по каждой реакции составляем расчетную табличку для отыскания ДМ и ДАЛ Деля - ДЛ1 на Т и складывая с AN, получаем gKp искомой реакции. [16]
Исходя из этой схемы реакций получается [103] весьма сложное выражение для брутто-скорости реакции окисления азота, которое включает различные комбинации 9 констант, соответствующих приведенным элементарным процессам. Такие сложные выражения не могут быть использованы для анализа и сопоставления с опытными данными. Поэтому в работе [103] делается попытка на основе различных приближений получить более простое уравнение скорости реакции, которое позволило бы вывести зависимость скорости реакции от константы, характеризующей рекомбинацию ионов при повышенных давлениях. [17]
Сопоставление величин потенциалов появления ионов азота и потенциалов начала реакции показывает, что реакция окисления азота начинается с образования ионов N, которые способны вступать во взаимодействие с молекулярным кислородом. [18]
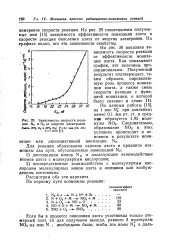 |
Зависимость скорости реакции М2 и О2 от энергии электронов. [19] |
На рис. 29 сопоставлены полученные ими [15] зависимости эффективности ионизации азота и скорости реакции окисления азота от энергии электронов. На графике видно, что эти зависимости оимбатны. [20]
Добавка кислорода в основном нужна не для процесса сжигания топлива, а для интенсификации реакции окисления азота и повышения концентрации этих окислов в газе. Быстрое охлаждение продуктов сгорания до 1500 С происходит в конвективно-испарительных газоходах парогенератора. [21]
Построение соответствующего графика ( рис. 53) убеждает в том, что энергия активации реакции окисления азота очень близка к нулю, так как даже совсем малое значение ЕО 200 кал / моль дает вполне заметный наклон прямой. [22]
В этом отношении несомненный интерес представляют многочисленные исследования по применению высокочастотных разрядов для проведения реакции окисления азота. [23]
На рис. 28 видно, что при увеличении энергии электронов выше 24 эв скорость реакции окисления азота продолжает возрастать. Это обстоятельство связано с зависимостью эффективности ионизации азота от энергии электронов. [24]
Данный вывод подтверждается результатами о влиянии электрического поля, а также благородных газов на реакцию окисления азота. Эти результаты будут рас - % смотрены далее. [25]
Данный вывод подтверждается результатами о влиянии электрического поля, а также благородных газов на реакцию окисления азота. Эти результаты будут рассмотрены далее. [26]
Сопоставляя величины потенциалов появления ионов азота и потенциалов начала реакции, можно прийти к заключению, что реакция окисления азота начинается при образовании ионов Na, которые, по-видимому, способны вступать в непосредственное взаимодействие с молекулярным кислородом. [27]
Сопоставляя величины потенциалов появления ионов азота и потенциалов начала реакции, можно прийти к заключению, что реакция окисления азота начинается при образовании ионов Ng, которые, по-видимому, способны вступать в непосредственное взаимодействие с молекулярным кислородом. [28]
В табл. IX-13 приведены рассчитанные в интервале температур 298 - 2000 К значения равновесных парциальных давлений кислорода для всех реакций окисления азота. [29]
Когда температура достигает 3000 К и выше, существенное влияние на процесс теплообмена начинает оказывать диссоциация составляющих воздух газов ( азота и кислорода), а также реакции окисления азота, окислы которого затем также диссоциируют. При температуре 5000 - 6000 К начинается ионизация воздуха: появляются ионы атомарного кислорода и азота, ионы окиси азота и свободные электроны. [30]
Страницы: 1 2 3 4