Реакция - полное окисление
Cтраница 3
Процесс протекает при давлении 3 2 - 8 5 am; при более высоком давлении в основном протекают реакции полного окисления, которые приводят к образованию окиси и двуокиси углерода. Оптимальная температура реакции 380 - 400 С; продолжительность нагрева при этой температуре - от 1 0 до 1 51 сек. Степень превращения 40 %, из которых 15 % составляют полезные продукты. [31]
 |
Средние температуры некоторых пламен. [32] |
Внутренняя восстановительная область отделена от внешней окислительной реакционной зоной - внутренним конусом, в котором реально и протекают реакции полного окисления. Реакционная зона окрашена в зеленовато-голубой цвет, вследствие излучения молекулярных полос радикала С2, кроме того, в ней присутствуют молекулы N2) O2, СО и другие. Их излучение практически перекрывает весь спектр, поэтому внутренняя восстано вительная область не может быть использована для аналитических целей. Внешняя область пламени содержит нагретые до высокой температуры продукты полного сгорания углеводородов, газы воздуха, радикалы и вследствие равновесности реакций также некоторые количества СО, Н, О. Она интенсивно излучает в инфракрасной области спектра и мало излучает в видимой и ультрафиолетовой областях, что делает ее удобным источником эмиссии атомных спектров элементов. [33]
 |
Схема окисления этилена в кипящем слое катализатора. [34] |
Интенсивный отвод реакционного тепла в этом процессе весьма важен, так как при температуре выше 300 С ускоряется реакция полного окисления этилена до двуокиси углерода и воды. Реакционное тепло отводится циркулирующими высококипящими органическими теплоносителями или испаряющейся водой в межтрубном пространстве контактного аппарата. Возможность эффективного съема тепла, образующегося при реакции, является одним из самых сложных вопросов при промышленном осуществлении каталитического окисления этилена. [35]
В присутствии окиси хрома [413, 414] и хроматов магния [416-418, 420-421], меди [416-418, 420], железа [416, 417], никеля [416] ускоряются главным образом реакции полного окисления парафинов, цикланов, олефинов. Индивидуальная окись хрома [442] слабо, а окись хрома в составе железо-хромовых окисных катализаторов [442-456], промотированных добавками щелочных и щелочноземельных металлов [457-459], более активно ведут процесс конверсии СО в СО2 в присутствии водяных паров. [36]
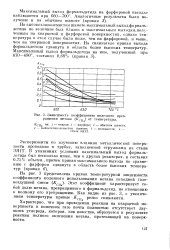 |
Зависимость коэффициента полезного превращения метана ( Л ( ц от температуры. [37] |
Характерно, что при проведении реакции на кварцевой поверхности в конечном газе почти полностью отсутствует двуокись углерода, которая, как известно, образуется в результате реакции полного окисления метана, протекающей на поверхности. [38]
Принимая во внимание только эти две реакции, при 50 % - ной конверсии этилена в окись этилена и такой же конверсии в продукты горения на реакцию полного окисления приходится около 91 % всего выделившегося тепла. Даже при 60 % - ной конверсии в окись этилена, чего достичь исключительно трудно, при образовании 1 кг окиси этилена выделяется 5500 ккал благодаря одновременному протеканию реакций горения. [39]
Тщательное регулирование температуры имеет очень большое значение, так как уменьшение ее ниже 60 - 70 С приводит к накоплению перуксусной кислоты, а повышение - к усилению побочных реакций, в частности реакции полного окисления ацетальдегида. [40]
Давление не влияет на селективность процесса, но она сильно зависит от температуры и степени конверсии этилена. Реакции полного окисления имеют более высокую энергию активации, и поэтому при постоянной степени конверсии селективность падает с повышением температуры ( рис. 101 а, стр. В свою очередь, при постоянной температуре селективность является функцией степени конверсии этилена. Поскольку температура реакции и степень конверсии влияют также на скорость процесса и производительность установки, выбор оптимальных условий определяется совокупностью всех факторов. Оптимальной температурой считается 220 - 280 С. Более низкой температуре должно соответствовать более высокое рабочее давление, чтобы производительность реактора сохранялась на высоком уровне. [41]
Закономерности подбора катализаторов для некоторых реакций не удается объяснить с помощью теории кристаллического поля, хотя для них обнаруживается двухпиковая картина изменения активности. Примером является реакция полного окисления различных веществ. Иногда при подборе катализаторов наблюдаются закономерности, противоположные предсказанным на основе теории кристаллического поля. В ряде случаев двухпиковую зависимость можно объяснить, привлекая представления о том, что в лимитирующей стадии происходит перенос заряда от ли-ганда в d - зону металла. Сомнения в правильности двухпиковой зависимости теория кристаллического поля вызывает еще и потому, что согласно этой теории в большинстве случаев в качестве лимитирующей стадии необходимо принять хемосорбцию, что противоречит экспериментальным данным. [42]
Большое влияние на режим работы реактора оказывает реакция полного сгорания этилена, тепловой эффект которой более чем в 10 раз больше теплового эффекта основной реакции. Для замедления реакции полного окисления к сырью добавляют такие ингибиторы, как те-траэтилсвинец, дибромэтан, бензол, этанол, хлорбифе-нил, хлорполифенил. [43]
Большое влияние на режим работы контактного аппарата оказывает реакция полного окисления этилена, тепловой эффект которой почти в 10 раз больше теплового эффекта основной реакции. Для замедления реакции полного окисления к исходному сырью добавляют такие ингибиторы, как тетраэтилсвинец, ди-бромэтан, бензол, этанол, хлордифенил, хлорполифенил, этилен-хлоргидрин, а при работе в кипящем слое используют твердые галогенпроизводные. [44]
В этом случае из-за кинетического ограничения реакция синтеза окиси этилена практически реализуется только до небольших глубин превращения. При углублении процесса усиливается реакция полного окисления этилена до воды и углекислого газа. [45]
Страницы: 1 2 3 4