Реакция - полиамидирование
Cтраница 2
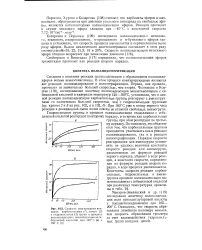 |
Скорость реагирования концевых карбоксильных ( /, амино - ( 2 и гидроксильных ( 3 групп в процессе поликонденсации моноэтаноламина себациновой кислотой при 120 С ( а и 160 С ( б. [16] |
По-видимому, это объясняется тем, что карбоксильным группам приходится участвовать как в реакции полиамидирования, так и в реакции полиэтерификации. Порядок скорости реагирования для аминогрупп установить не удалось: величина константы скорости реакции для аминогрупп, рассчитанная по формуле реакций первого порядка, убывает в ходе реакции, а константа скорости, определенная по формуле реакции второго порядка, в ходе процесса увеличивается. [17]
Из эндотермического характера поликонденсационного процесса следует, что с повышением температуры константа равновесия реакции полиамидирования будет увеличиваться. Поэтому в состоянии равновесия молекулярная масса полиамида должна возрастать с повышением температуры. Практически это не наблюдалось, так как обычно очень трудно выделить этот эффект в чистом виде, поскольку повышение температуры приводит и к другому эффекту - ускоряет приближение системы к состоянию равновесия и облегчает удаление низкомолекулярного вещества. [18]
Как было раньше установлено, в работах нашей лаборатории [ и 12 энергия активации реакции полиамидирования выше энергии активации полиэтерификации. Однако в условиях совместной поликонденсации энергетически более выгодной оказывается реакция образования амидных связей. Это можно объяснить тем, что взаимодействию гидро-ксильных групп с карбоксильными в присутствии аминогрупп должен предшествовать разрыв гетерополярной связи между карбоксильными и аминогруппами, на что требуется около 13 ккал. [19]
САо - начальная концентрация вещества А ft - порядок реакций, 1 - константа скорости реакций полиамидирования, % - время, приводит к значительным трудностям при аналитическом решении. [20]
В частности, представляют интерес реакции взаимодействия аминов с ангидридами органических кислот, поскольку они аналогичны некоторым реакциям полиамидирования. [21]
Поэтому здесь будут отмечены лишь некоторые работы, опубликованные за период 1953 - 1956 гг. и посвященные частным случаям реакции полиамидирования. В табл. 1 и 2 приведены материалы о поликонденсации диаминов с дикарбоновыми кислотами и их производными и поликонденсации аминокислот и их производных. [22]
Кроме перечисленных соединений очень эффективными активаторами являются щелочи и металлический натрий, которые в десятки и сотни раз сокращают продолжительность реакции полиамидирования. [23]
На рис. 89 показано изменение коэффициента полимеризации полиамида во времени при различных температурах, а на рис. 90 - изменение с температурой величины константы скорости реакции полиамидирования. Из данных рис. 90 можно видеть, что лишь в известном интервале температур ( 160 С и выше) константа скорости реакции полиамидирования изменяется в согласии с уравнением Аррениуса. При более низких температурах наблюдается значительное отклонение от уравнения Аррениуса. Челнокова, Рафиков и Коршак [71] объясняют это влиянием резкого повышения вязкости реакционной среды при более низких температурах. Энергия активации полиамидирования гексаметилендиамина и себациновой кислоты, вычисленная па основании того участка кривой ( см. рис. 90), где применимо уравнение Аррениуса, равна 24 ккал / моль. [24]
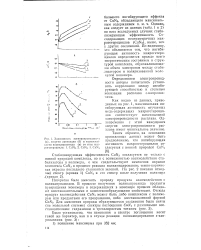 |
Зависимость электропроводноста ( а, энергии активации ( б и термостойкости поликапроамида ( в от типа мак-рогстероцикла. 1. CuN3, 2. CuNa, 3. CuN (. [25] |
Стабилизирующая эффективность CuN3 согласуется не только с ионной природой комплекса, но и с возможностью взаимодействия стабилизатора и полимера, о чем свидетельствуют изменения окраски комплекса CuN3 в процессе реакции полиамидирования; темно-коричневая окраска последнего становится зеленой. [26]
В реакционную колбу, снабженную электромеханической мешалкой и обратным холодильником, помещают 26 6 г ( 0 1 моль) соли АГ и 25 мл ж-крезола. Реакцию полиамидирования проводят при 210 - 220 С на бане со сплавом Вуда. Непосредственно перед растворением соли в реактор пропускают ток инертного газа. Через 60 и 120 мин после растворения соли по методике, описанной в работе I. Затем расплав выливают в термостойкий стакан ( на 200 мл) и добавляют 100 мл муравьиной кислоты. [27]
Другая характерная особенность поликапроамида заключается в том, что при его получении в трубах непрерывной полимеризации реакция между реакционноспособными группами NH2 и СООН мономеров не заканчивается и эти группы остаются в полимере. Поэтому реакция полиамидирования продолжается и во время формования волокна вплоть до охлаждения расплавленых струек в прядильной шахте. Вследствие этого молекулярный вес полимера и вязкость расплава продолжают увеличиваться, что нарушает стабильность процесса формования. [28]
Наиболее эффективным катализатором из числа использованных в качестве добавок веществ является борная кислота. Ускоряя реакцию полиамидирования, борная кислота в то же время является мало эффективным стабилизатором макромолекул полиамида, что приводит к получению более высокомолекулярных полиамидов, чем при поликонденсации в тех же условиях в присутствии других катализаторов. [29]
Линейные преполимеры легко образуются в тех случаях, когда функциональные группы в мономерах, находящиеся в ор mo - положениях друг к другу, значительно различаются по реакционной способности [ напр. При этом реакции полиамидирования протекают в условиях, аналогичных условиям синтеза ароматич полиамидов. [30]
Страницы: 1 2 3