Реакция - бутадиен
Cтраница 3
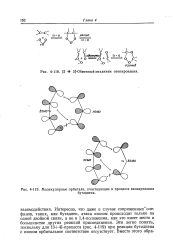 |
Молекулярные орбитали, участвующие в процессе озонирования. [31] |
Интересно, что даже в случае сопряженных Ъле-финов, таких, как бутадиен, атака озоном происходит только по одной двойной связи, а не в 1 4-положения, как это имеет место в большинстве других реакций присоединения. Это легко понять, поскольку для [3 4] - процесса ( рис. 4 - 119) при реакции бутадиена с озоном орбитальное соответствие отсутствует. [32]
Для стабилизации каучука в латекс добавляется неозон Д ( фенил - 3-нафтиламин), который вводится в последний реактор в виде раствора в количестве 2 - 3 % от веса каучука. Из этого раствора латекс направляется в сборник, где давление снижается до 0 2 ат, благодаря чему из латекса выделяется основное количество не вошедшего в реакцию бутадиена, пары которого далее сжижаются под давлением 4 ат. [33]
Реакция Дильса-Адлера представляет собой более сложный тип реакции циклизации. Из большого числа реакций этого типа, изученных различными авторами 24, в табл. 12 приводятся значения энергии активации и предэкспонента для двух наиболее простых реакций - реакции бутадиена с этиленом и бутадиена с бутадиеном. [34]
Наиболее общим условием, рекомендуемым для синтетических работ, является нагревание в течение 10 - 30 час. Важно помнить, что во многих случаях с реакцией Дильса-Альдера конкурирует реакция свободно-радикальной со-полимеризации олефинов и диолефинов, поэтому часто желательно добавление в такие системы антиокислителей. В качестве примера такой конкурирующей реакции ( при соответствующим образом подобранных условиях) может служить реакция бутадиена и акрилонитрила, приводящая к образованию каучукоподобного полимера или тетрагидробензо-нитрила. Кроме того, как будет показано, конденсации по Дильсу-Альдеру - практически обратимые реакции, поэтому продукты конденсации могут распадаться при более высоких температурах. Однако температура, при которой происходит пиролиз, и выход регенерированного исходного вещества колеблются в широких пределах для разных систем. Некоторые из факторов, влияющих на это, будут обсуждены ниже более детально. [35]
Вследствие большого количества продуктов реакции ( выше 32 отдельных веществ) установка должна иметь секцию разделения компонентов и очистки бутадиена. Промышленный метод состоит из следующих операций: каталитическое превращение этилового спирта в бутадиен; разделение жидких компонентов ( в нормальных условиях); выделение из газов реакции неочищенного бутадиена при помощи абсорбции этиловым спиртом и очистка бутадиена. [36]
Приведенный обзор современного состояния вопроса и дальнейших возможностей даны в статье Стокиса, Шефилда и Фрэнклина, которые касались таких производных бутадиена, как тетрагидро-и гексагидрофталевые кислоты, малеиновый ангидрид, н-бутил-бензол, винилциклогексен-4 ( димер, получаемый полимеризацией бутадиена-1 3 в присутствии медного или хромового катализаторов), тетрагидробензальдегид, эритрит и изосебациновые кислоты. По оценке авторов, для удовлетворения потребности во всех этих продуктах достаточно 1500 т бутадиена в год. Одна установка для получения этих кислот уже находится в действии. Весьма перспективные реакции бутадиена типа Дильса - Альдера заслуживают дальнейшего изучения. [37]
Если бутадиен и этилен реагируют, находясь в параллельных плоскостях ( схема 25.8), то такая реакция разрешена в основном электронном состоянии. Корреляционная диаграмма молекулярных орбиталей приведена на схеме 25.8. Видно, что в отличие от димеризации этилена, здесь не наблюдается подъема электронных пор к антисвязывающим уровням. Тем не менее, случай реакции этилена с бутадиеном показывает, что термин разрешена вовсе не обязательно означает, что реакция идет в прямом смысле легко. По расчету для реакции незамещенного бутадиена с незамещенным этиленом энергия активации равна 34 ккал / моль; это очень большая величина. По-видимому, высокая энергия активации связана с тем, что необходимо затратить большую энергию на растяжение трех двойных связей СС, которые в продукте реакции должны стать простыми связями. [38]
По мере сближения реагентов энергия взаимодействия увеличивается. Как видно из рис. 13.15, рассчитанный путь реакции связан с одновременным и равномерным сближением соответствующих центров. Это и есть условие согласованной и притом синхронной реакции циклоприсо-единения. Указанный результат подтвержден строгими ab initio расчетами ППЭ реакции бутадиена с этиленом. [39]
Вилке 2 ], однако до настоящего времени данные по изучению этой реакции носят в основном патентный характер, зачастую противоречивый. Кроме того, з литературе отсутствуют сведения о сравнительной активности каталитических систем i реакции циклотримеризацпи бутадиена. [40]
Электролизеры представляют собой аппараты без диафрагмы с платино-титановьши анодами. Напорный бак, трубопроводы и электролизер также снабжены теплоизоляцией. В этом холодильнике метанол и бутадиен практически полностью конденсируются. Продукты электролиза, представляющие собой растворенную в метаноле смесь диэфиров высших ненасыщенных дикарбоновых кислот, диэфира себациновой кислоты, эфиров легких карбоновых кислот с не вступившей в реакцию солью монометиладипината, из последнего электролизера каскада поступают в параллельно включенные сборники 12, где производится последовательная отгонка не вступившего в реакцию бутадиена и метанола. Пары бутадиена и метанола, пройдя через холодильник 13, конденсируются и собираются в сборнике 14, откуда конденсат поступает в смеситель 6, где производится приготовление электролита. Продукты, оставшиеся в сборниках 12 после отгонки бутадиена и метанола, смешиваются с водой для растворения соли монометиладипината. При этом образуются два слоя - нейтральные продукты электролиза и водный раствор соли моноэфира. Далее смесь поступает в отстойники 15, где происходит отделение водного слоя от органического. [41]
Приведенный обзор современного состояния вопроса и дальнейших возможностей даны г, статье Стокиса. Шефилда и Фрэнклина, которые касались таких производных бутадиена, как тетрагидро-и гексагидрофталевые кислоты, малеиновый ангидрид, w - бутил-бензол, винилциклогексен-4 ( димер, получаемый полимеризацией бутадпена-1 3 в присутствии медного или хромового катализаторов), тетрагидробензальдегид, эритрит и изосебациновые кислоты. По оценке авторов, для удовлетворения потребности во всех этих продуктах достаточно 1500 т бутадиена в год. Одна установка для получения этих кислот уже находится в действии. Весьма перспективные реакции бутадиена типа Дильса - Альдера заслуживают дальнейшего изучения. [42]
Технология фирмы du Pont включает гидроцианирование бутадиена в присутствии катализатора, содержащего металлический никель. На первой стадии происходит присоединение синильной кислоты к бутадиену с образованием смеси изомерных ненасыщенных мононитрилов. Продукты реакции разделяют и нитрилы изостроения подвергают изомеризации; полученную равновесную смесь изомеров снова разделяют. Затем проводят присоединение второй молекулы синильной кислоты и из образовавшейся смеси динитрилов выделяют адипонитрил. В основе процесса фирмы Esso лежит реакция бутадиена с иодом и цианистой медью, приводящая к получению комплекса дегидроадипонит-рила с иодидом одновалентной меди. При гидролизе этого комплекса водным раствором синильной кислоты с высоким выходом образуется дегидроадипонитрил и регенерируются иод и цианистая медь, которые возвращают в реакцию. [43]
ППЭ, ъ которой энергетическая характеристика представлена энергией взаимодействия. На рис. 119 представлен участок ППЭ реакции бутадиена с этиленом, соответствующий сближению реагентов в конфигурации типа X. По мере сближения реагентов энергия взаимодействия увеличивается. Как видно из рис. 119, рассчитанный путь реакции связан с одновременным и равномерным сближением соответствующих центров. Это и есть условие согласованной и притом синхронной реакции циклоприсоединения. Указанный результат подтвержден строгими ab initio расчетами ППЭ реакции бутадиена с этиленом. [44]
Страницы: 1 2 3