Реакция - электрофильное присоединение
Cтраница 3
Реакция является реакцией электрофильного присоединения. [31]
Способность олефииов к реакции электрофильного присоединения определяется плотностью электронов у двойной связи. Последовательное замещение атомов водорода у двойной связи на электро-нодонорные метильные группы увеличивает электронную плотность у двойной связи [5] и, следовательно, увеличивает скорость реакции эпоксидирования. [32]
Надкислоты вступают в реакции электрофильного присоединения с олефинами, которые очень напоминают реакции карбенов ( разд. Особенно легко таким атакам подвергаются енольные эфиры. Для введения в эту реакцию соединения с сопряженными двойными связями необходимо дейст вие сильных надкислот. [33]
Если бы все реакции электрофильного присоединения хлора проходили через классический ион карбония, который образуется прямо из электрофила и олефина и в котором были бы неважны взаимодействия между карбониевым центром и связанным заместителем, то нельзя было бы ожидать, что продукты сильно зависят от природы электрофила, начинающего атаку. Данные об ионах карбония, полученных другими путями ( гл. В действительности следует ожидать, что осложнения реакционного процесса, связанные с участием нескольких последовательных промежуточных соединений [ уравнение ( 6 - 10) ], будут проявляться в изменении природы продуктов. Что касается ориентации продуктов, то здесь изучено мало примеров, и результаты несколько противоречивы. Два возможных продукта присоединения хлорноватистой кислоты к хлористому аллилу [5] образуются в примерно равных количествах; следовательно, ведущие к ним переходные состояния не могут сильно отличаться по свободной энергии активации. Продукты реакции изучались в условиях, которые должны обусловливать инициирование реакции положительным галогеном, хлором и моноокисью хлора. [34]
Подробное кинетическое изучение реакций электрофильного присоединения началось сравнительно недавно, и вполне очевидно, что новые результаты могут привести к существенному уточнению ( а может быть, и изменению) наших представлений о механизмах этих реакций. [35]
Изучение большого числа реакций электрофильного присоединения позволило сделать вывод, что реакция может протекать по одному из трех следующих механизмов. [36]
Для алкенов особенно типичны реакции электрофильного присоединения; нуклеофильные реакции легко осуществляются с замещенными алкенами, в которых двойная связь активирована сопряжением с электрофильными группами ( стр. [37]
 |
Схема молекулярных орбиталей этилена. [38] |
В рамках теории МО реакция электрофильного присоединения брома к этилену может быть описана следующим образом. [39]
Типичны ли для бензпирена реакции электрофильного присоединения. [40]
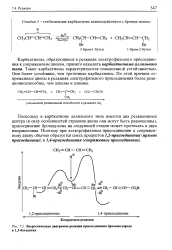 |
Энергетическая диаграмма реакции присоединения бромоводорода к 1 3-бутадиену. [41] |
Карбкатионы, образующиеся в реакциях электрофильного присоединения к сопряженным диенам, принято называть карбкатионами аллильного типа. Такие карбкатионы характеризуются повышенной устойчивостью. Они более устойчивы, чем третичные карбкатионы. По этой причине сопряженные диены в реакциях электрофильного присоединения более реак-ционноспособны, чем алкены и алкины. [42]
Правило Марковникова - в реакциях электрофильного присоединения алкенов протон реагента преимущественно присоединяется к более гидрогенизированному атому углерода. [43]
В каком направлении преимущественно протекают реакции электрофильного присоединения. [44]
Общая для всех этих процессов реакция электрофильного присоединения протона или другого электрофила по двойной связи не является одностадийной - присоединению всегда предшествует образование я-комплекса электрофила с олефином. [45]
Страницы: 1 2 3 4