Реакция - разрыв
Cтраница 3
Терпеновые углеводороды обнаруживают общую для них способность к катализируемой кислотами реакции разрыва кольца. [31]
Оставалось неясным, почему предполагаемая локализация зарядов должна создавать движущую силу реакции разрыва, поскольку ионизация тем или иным способом влияет на всю молекулу ( разд. По-видимому, здесь определяющей особенностью процесса является устойчивость продуктов реакции. [32]
В последние годы в результате исследования пиролитических процессов наши знания о реакциях разрыва простых связей значительно расширились. Было найдено, что во многих случаях энергия активации разрыва связи Е равна энергии разрыва связи D, что позволило измерить энергии связей ( рис. 7) и исследовать факторы, определяющие эту величину. Энергия разрыва связи определенного типа, например связи С-С, не является постоянной величиной, а определяется влиянием атомов или групп, находящихся у этой связи. D) связей С-С, показывает, что эта энергия может изменяться в значительных пределах. [33]
В низкотемпературной области вместе с простым испарением низкомолекулярных летучих компонентов возможно протекание реакций разрыва основной цепи и структурирования. При этом весовые потери во второй температурной области обусловлены в значительной степени чисто термическим процессом. Кислород лишь ускоряет структурирование полиорганосилоксанов и способствует образованию активных центров деполимеризации. [34]
Установлено, что основной реакцией взаимодействия хитоэана о HgOg в мягких условиях является реакция разрыва гликозидных связей, предположительно, по радикальному механизму. [35]
В настоящее время не установлено, действует ли кислород главным образом путем ускорения реакции разрыва или путем замедления сшивания. Из изложенного выше ясно, что он не ускоряет разрыва цепей таких полимеров, как полиизобутилен и полиметилметакрилат, где деструкция протекает быстро и является единственной реакцией. Однако он может ускорять деструкцию других полимеров, например за счет проникновения в клетки Франка - Рабиновича и блокирования полимерных радикалов, возникающих при разрыве цепей. Получены [24] некоторые доказательства, что в отношении полистирола и полиэтилена действие кислорода проявляется главным образом в ускорении деструкции, причем скорость сшивания не изменяется. [36]
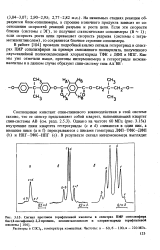 |
Сигнал протонов терефталевой кислоты в спектрах ПМР сополиэфира бис ( 4-оксифенил - 2 2-пропана, неопентилгликоля и хлорангидрида терефталевой кислоты. [37] |
На начальных стадиях реакции образуются блок-сополимеры, а строение конечного продукта зависит от соотношения скоростей реакций разрыва и роста цепи. Если эти скорости близки ( системы с ЭГ), то получают статистические сополимеры ( 8s 1); если скорость роста цепи превышает скорость разрыва ( системы с тетра-метиленгликолем), то сохраняется блочное строение сополимера. [38]
Алкил-1 2 3 4-тетрагидронафталины ( тетралины) в условиях гидродеалкилирования, как и рассмотренные выше алкилинданы, вступают в реакции разрыва насыщенного кольца и гидродеалкилирования боковых цепей. [39]
В / 1 / на примере спиртов показано, что времена Ю - И - кЮ с характерны для реакций разрыва, образования и переноса межмолекулярных водородных связей. [40]
На уровне теории UCCSD ( T) / / UCCD / cc-p VDZ рассчитан энергетический профиль синглетной ППЭ вдоль координаты реакции разрыва О - О-связи в диметилпероксиде. Равновесной структуре МеООМе С2 - симметрии на используемом уровне теории отвечает торсионный угол С - О - О - С, равный 117.9, длина связи С - О - 1.415 А, а длина пероксидной связи - 1.442 А. [41]
В условиях каталитического крекинга ( температура 450 - 550 СС, давление 0 1 - 0 3 МПа, катализатор) протекает большое число реакций, среди которых определяющее влияние на результаты процесса оказывают реакции разрыва углерод-углеродной связи, перераспределения водорода, ароматизации, изомеризации, разрыва и перегруппировки углеводородных колец, конденсации, полимеризации и коксообразова-ния. [42]
Найдено, что энергия активации реакции сшивания поливинилового спирта при облучении равна 7 5 ккал / моль на воздухе и 2 7 ккал / моль в вакууме при температурах 100 С, а энергия активации реакции разрыва основной цепи полимера - 2 0 ккал / моль на воздухе и 2 2 ккал / моль в вакууме. [43]
Неравновесная ноли конденсация имеет место, во-первых, в том случае, когда процесс протекает при низких температурах, вследствие чего скорость обменных и деструктивных реакций равна нулю, и, во-вторых, когда связи, образующиеся в результате реакции, столь прочны, что протекание каких бы то ни было реакций разрыва этих связей исключено. [44]
 |
Диаграмма комплексной диэлектрической проницаемости w - пропанола при 40 и - 80 С. [45] |
Страницы: 1 2 3 4