Реакция - рассматриваемый тип
Cтраница 2
Роль временного параметра в реакциях рассматриваемого типа играет линейная скорость потока, рассчитываемая как отношение объема парогазовой смеси ( метанол, вода, воздух), прошедшего за единицу времени, к площади сечения реактора. Лишь при предельно низких линейных скоростях конверсия метанола возрастает. И лишь при увеличении линейной скорости примерно на порядок и конверсия, и селективность образования начинает падать, теперь уже вследствие постепенного смещения системы во внекаталитическую область. Отмеченные зависимости наглядно видны и в том случае, когда вместо линейной скорости потока в качестве аргумента принимают пропорциональную ей величину, называемую нагрузкой по метанолу, и выражают массой последнего, которая подается на единицу сечения реактора в единицу времени. Очевидно, что нагрузка по метанолу наглядно характеризует производительность катализатора. Сопоставление этой величины с объемной скоростью процесса в кинетической области ( 0 2 ч - 1) свидетельствует о том, что производительность серебряного катализатора во внешнедиффузионной области примерно на 2 порядка выше, чем в кинетической. Это соотношение примерно соблюдается и при сравнении производительности серебряного контакта с железомолибденовым. [16]
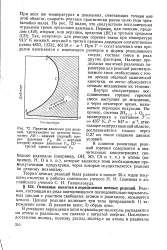 |
Пределы давления для реакций, протекающих по цепному механизму. АВ - нижний ( первый предел давления Plt ВС - верхний ( второй предел давления Р2, CD - третий предел давления Р3. [17] |
Наличие предельных значений различных параметров для реакций рассматриваемого типа необъяснимо с тоу-ки зрения обычной химической кинетики, но легко объясняется цепным механизмом их течения. Внутри полуострова воспламенения горение горючей смеси наступает не мгновенно, а через некоторое время, называемое периодом индукции. [18]
Медленное самоускорение, наблюдающееся в случае реакций рассматриваемого типа, объясняется существованием особого рода разветвлений - вырожденных. Вырожденное разветвление представляет собой образование активных центров ( свободных атомов и радикалов) в результате сравнительно редких реакций лабильных молекулярных промежуточных веществ. Так, например, редкий распад перекисных соединений ROOH с разрывом слабой перекисной связи - О-О -, приводящий к образованию алкоксильного радикала RO и свободного гидроксила ОН, является вырожденным разветвлением. Так как образование радикала в этом случае происходит редко, процесс хотя и будет ускоряться по мере накопления продукта, разветвляющего цепи, самоускорение это будет медленным. Для медленно самоускоряющихся цепных реакции также были открыты критические явления. [19]
Медленное самоускорение, наблюдающееся в случае реакций рассматриваемого типа, объясняется существованием особого рода разветвлений - вырожденных. Вырожденное разветвление представляет собой образование активных центров ( свободных атомов и радикалов) в результате сравнительно редких реакций лабильных молекулярных промежуточных веществ. Так, например, редкий распад перекисных соединений ROOH с разрывом слабой перекисной связи - О-О -, приводящий к образованию алкоксильного радикала RO и свободного гидроксила ОН, является вырожденным разветвлением. Так как образование радикала в этом случае происходит редко, процесс хотя и будет ускоряться по мере накопления продукта, разветвляющего цепи, самоускорение это будет медленным. Для медленно самоускоряющихся цепных реакций также были открыты критические явления. [20]
Расчет степени взаимодействия в системах с реакциями рассматриваемого типа основан на определении содержания продуктов реакции в равновесной смеси, исходя из аналитической связи между величинами свойств равновесной смеси г /, величинами свойств той же смеси в предположении отсутствия взаимодействия и при взаимодействии, прошедшем до конца. [21]
Таким образом, согласно современным представлениям относительно реакций рассматриваемых типов, они могут протекать как по гемолитическому, так и по ионному механизму в зависимости от реакционной системы и величины анодного потенциала. Не исключена возможность смешанного механизма, как. [22]
Следует отметить некоторые особенности, характерные для всех реакций рассматриваемого типа. После стадии инициирования ( инициирование может быть вызвано различными способами в зависимости от условий реакции) следуют две стадии роста цепи, одна из которых представляет присоединение к двойной связи, а вторая - свободнорадикальное замещение. В противоположность этому полимеризация состоит из ряда реакций присоединения, а галогениро-вание углеводородов - из ряда чередующихся реакций замещения. Другой существенный момент заключается в том, что присоединение по двойной связи осуществляется у ее конца, наименее затрудненного сте-рически; при радикальном замещении предпочтительнее атака на незатрудненные атомы, типа галогена или водорода, находящиеся на периферии молекулы, чем на атом углерода в центре молекулы. Необходимое условие - высокая скорость стадий роста цепи - означает, что эти стадии должны быть экзотермическими и что осуществление этих стадий не должно сопровождаться преодолением значительного сте-рического барьера. [23]
Наличие кинетического изотопного эффекта является - характерным отличием реакций рассматриваемого типа от кислотно-каталитических процессов, рассмотренных в предыдущем разделе, в которых лимитирующей стадией является превращение иротонизованной формы. [25]
Изображенное на этой схеме циклическое переходное состояние в реакциях рассматриваемого типа тем более вероятно, чем менее полярен растворитель. [26]
В этом отношении можно сопоставить все описанные в литературе реакции рассматриваемого типа. При этом наблюдается следующая картина. [27]
В заключение следует напомнить, что влияние давления на скорость реакций рассматриваемого типа складывается из двух эффектов - эффекта увеличения концентрации и влияния давления на константу скорости реакции. При температурах, значительно превышающих критические температуры реагирующих газов, и не очень высоких давлениях первый эффект является доминирующим. По мере приближения плотности газовой смеси к плотности жидкостей влияние давления на константу скорости реакции становится все более значительным. [28]
Превращение карбоновых кислот в хлорангидриды и ангидриды также относится к реакциям рассматриваемого типа и осуществляется при обработке их пента - или трихлори-дом, а также хлороксидом фосфора и тионилхлоридом. Реакция протекает через стадию образования производного, в котором атом водорода в карбоксильной группе замещен на сильную электроноакцепторную группировку. [29]
В настоящей работе будут приведены аргументы в пользу гипотезы о резонансном характере реакций рассматриваемого типа. Указанное предположение относится и к некоторым другим неупругим бимолекулярным процессам. Парциальные ширины различных каналов реакций определяются только свойствами конкретной системы, на них не налагаются какие-либо общие соотношения ( в отличие от теории равновесного комплекса), поэтому наше предположение не противоречит рассмотренным экспериментальным данным. [30]
Страницы: 1 2 3 4
