Реакция - третье - порядок
Cтраница 1
 |
Зависимость константы скорости от температуры для реакции превращения цианата аммония в мочевину. [1] |
Реакции третьего порядка встречаются реже, чем реакции первого и второго порядка. Это объясняется малой вероятностью одновременной встречи трех молекул в пространстве. В реакции третьего порядка принимают участие молекулы одного вещества или различных веществ или две молекулы одного вещества и одна - другого. [2]
Реакция третьего порядка соответствует столкновению трех частиц. [3]
Реакции третьего порядка встречаются очень редко и потому не имеет смысла рассматривать математический вывод их кинетического уравнения. [4]
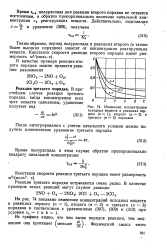 |
Изменение концентрации исходных веществ в реакциях первого ( л 1, второго ( п 2 и третьего ( п 3 порядков. [5] |
Реакции третьего порядка встречаются очень редко. [6]
Реакции третьего порядка вследствие низкой скорости их имеют малое практическое значение. [7]
Реакции третьего порядка встречаются сравнительно редко. В этом случае скорость реакции пропорциональна произведению трех концентраций. Реакции, скорость которых не зависит от концентрации реагирующих веществ, называются реакциями нулевого порядка. [8]
Реакции третьего порядка вследствие небольшой скорости имеют малое практическое применение. [9]
Реакции третьего порядка встречаются очень редко и потому не имеет смысла рассматривать математический вывод их кинетического уравнения. [10]
Реакции третьего порядка весьма редки. Было также показано, что рекомбинации атомов ( например. [11]
Реакции третьего порядка относительно немногочисленны. Третий порядок обычно характерен для побочных реакций. [12]
Реакции третьего порядка встречаются более редко, так как вероятность одновременного столкновения трех молекул значительно меньше. [13]
Реакции третьего порядка редки. [14]
Реакции третьего порядка вследствие малой скорости их имеют малое практическое значение. [15]
Страницы: 1 2 3 4