Реакция - электролиз
Cтраница 1
Реакции электролиза являются такими же химическими реакциями, как и все остальные. Поэтому по реакциям электролиза можно производить стехиометрические расчеты точно так же, как это было сделано для других реакций. [1]
Реакция электролиза требует более высокого напряжения, чем реакция заряда. Начальному слабому выделению газа соответствует напряжение 2 3 В, среднему 2 4 В и сильному 2 5 В и выше. [2]
Реакция электролиза требует более высокого напряжения, чем реакция заряда. Начальному слабому выделению газа соответствует напряжение 2 3 б, среднему 2 4 в и сильному 2 5 в и выше. [3]
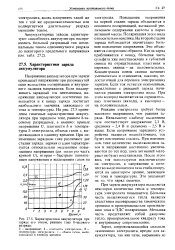 |
Характеристики аккумулятора при заряде его током, равным току 8-часового разряда. [4] |
Реакция электролиза требует более высокого напряжения, чем реакция заряда. Начальному слабому выделению газа соответствует напряжение 2 3 В, среднему - 2 4 В и сильному - 2 5 В и выше. [5]
Многие реакции электролиза не являются обратимыми. Наблюдаемый потенциал разложения превышает величину, вычисляемую из термодинамических данных. Этот избыточный потенциал, называемой потенциалом перенапряжения, зависит от площади электродов и состояния их поверхности, наличия примесей в растворе и плотности тока, протекающего через раствор. [6]
Многие реакции электролиза не являются обратимыми. [7]
Уравнения реакций электролиза являются такими же химическими уравнениями, как и все остальные уравнения реакций. [8]
Когда рассматриваются реакции электролиза в различных растворителях, условия, определяющие, какой ион будет разряжаться на каждом электроде, таковы, что нельзя вывести никаких определенных заключений относительно кислотно-основных явлений. Например, водород выделяется на катоде при электролизе водного раствора кислоты, но водород получается и тогда, когда электролизу подвергается водный раствор сульфата натрия или едкого натра. [9]
Напишите уравнение реакции электролиза, в которой в качестве исходною продукт 1, используется раствор хлорида натрия п получается хлор. Если в каждой электролизной ячейке за 24 ч производится 0 01 т хлора. [10]
Напишите уравнение реакции электролиза, в которой в качестве исходного продукта используется раствор хлорида натрия и получается хлор. Если в каждой электролизной ячейке за 24 ч производится 0 01 т хлора, какой ток ( в амперах) должен проходить через ячейку. [11]
Составляем уравнение реакции электролиза. [12]
Составьте уравнение реакции электролиза воды, при котором получается кислород. [13]
Составьте уравнение реакции электролиза воды, при котором получается кислород. [14]
Составим уравнения реакций электролиза водного раствора хлорида меди. [15]
Страницы: 1 2 3 4