Реакция - эпоксидирование
Cтраница 1
 |
Свойства эпоксихинондиоксимовой смолы. [1] |
Реакция эпоксидирования протекала при температуре 80 - 100 С в течение 1 5 - 3 час с пятикратным избытком эпихлоргид-рина. [2]
Реакция эпоксидирования описывается кинетическим уравнением, в котором концентрации циклооктадиена-1 5, гидроперекиси циклооктила и катализатора входят в первой степени. При восстановлении продуктов эпоксидирования окись циклооктадиена-1 5 превращается в циклооктанол, а непрореагировавший цик-лооктадиен-1 5 в циклооктан. Первый окисляют азотной кислотой в присутствии меднованадиевого катализатора в пробковую кислоту, а циклооктан направляют на окисление кислородом воздуха в гидроперекись циклооктила. [3]
Изучена реакция эпоксидирования 2 3-диметил - 2-бутена гидроперекисью трет-бутила в присутствии резината молибдена. Найдены условия, позволяющие получать окись ДМБ с количественным выходом на прореагировавшие олефин и гидроперекись. [4]
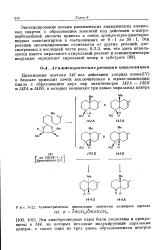 |
Асимметрическая циклизация оптически активного ацеталя 141. R СН ( СН3 СН ( ОН СН3. [5] |
Эти реакции эпоксидирования отличаются от других реакций, рассмотренных в последней части разд. [6]
В реакции эпоксидирования хлористого и бромистого аллилов надмалеиновой кислотой в широком диапазоне концентраций установлен первый порядок реакции по олефину. Галоидные аллилы окисляются труднее соответствующих симметричных дигалоидзамещенных олефинов. [7]
Изучена реакция эпоксидирования бутадиена-1 3 гидроперекисью изопрапил бензола в присутствии резината молибдена. Предложены условия проведения реакции, при которых конверсия гидроперекиси составляет 95 2 %, выход моноокиси бутадиена-1 3 на разложенную гидроперекись - 93 4 мол. [8]
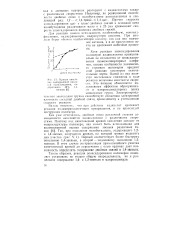 |
Кривая окисления надбснзойной кислотой полибутадиена, содержащего 40 % 1 4-звепьев. [9] |
Хотя реакция эпоксидирования полимеров надкислотами принципиально не отличается от эпоксидирования низкомолекулярных олефи-нов, однако особенности химического строения полимеров придают этой реакции некоторые отличительные черты. Одной из них является постепенное снижение в ходе реакции величины константы скорости. Это явление объясняется индуктивным эффектом образующихся в макромолекулярных цепях эпоксидных групп. Электроотрицательная эпоксидная группа способствует снижению электронной плотности соседней двойной связи, приводящему к уменьшению скорости реакции. [10]
Изучена реакция эпоксидирования бутадиена-1 3 гидроперекисью изопропил бензола в присутствии резината молибдена. Предложены условия проведения реакции, при которых конверсия гидроперекиси составляет 95 2 %, - выход моноокиси бутадиена-1 3 на разложенную гидроперекись - 93 4 мол. [11]
Изучена реакция эпоксидирования а-олсфинов органическими гидропероксидами в среде смешанного растворителя спирт-углеводород. Увеличение конверсии гидропероксида и выхода эгюксида в расчете на прореагировавший гид-ропероксид связано с влиянием спирта па протекание побочной реакции каталитического распада гидропероксида. Введение спирта также способствует снижению влияния продуктов реакции разложения на протекание целевой реакции. Изучена зависимость конверсии и селективности реакции от структуры ( первичный, вторичный, третичный) спирта. Показано влияние концентрации вводимого спирта на ход реакции эпоксидирования а-олефинов гидропероксидом изо-пропилбензола. [12]
Исследована реакция эпоксидирования аллилового спирта гидроперекисью изопропилбензола в среде различных технических растворителей. [13]
Исследована реакция эпоксидирования аллилового спирта гидроперекисью изопропилбензола в среде различных технических растворителей. [14]
Константа реакции эпоксидирования отрицательна, что доказывает электрофильный характер превращения. [15]
Страницы: 1 2 3 4