Реакция - эпоксидирование
Cтраница 2
Спирты в реакции эпоксидирования проявляют себя как ингибиторы каталитического распада гидропероксида, а также как активаторы и ингибиторы эпоксидирования олефинов. [16]
Изучено ингибирование реакции эпоксидирования трет-бутшто-вым спиртом. [17]
Изучено ингибирование реакции эпоксидирования трет-бутило-вым спиртом. [18]
Изучена кинетика реакции эпоксидирования циклогексена надуксуснои кислотой в широком интервале концентраций олефина. Подтвержден механизм реакции, предполагающий образование бимолекулярного промежуточного комплекса олефин-надкислота, и определены его термодинамические параметры. [19]
Исследованы закономерности реакции эпоксидирования 2-метилбутена - 2 гидропероксидом 2-метилбутана в присутствии тетрахлорида титана и тетрабутокеититана и выбраны условия для эффективного проведения реакции эпоксидирования. [20]
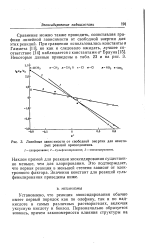 |
Линейные зависимости от свободной энергии для некоторых реакций присоединения. [21] |
Установлено, что реакция эпоксидирования обычно имеет первый порядок как по олефину, так и по над-кислоте в самых различных растворителях, включая уксусную кислоту и бензол. [22]
Активность перфторолефинов в реакции эпоксидирования находится в соответствии с активностью по отношению к действию нуклеофильных реагентов. Тот факт, что окиси перфторолефинов легко реагируют с фторид-анионом, позволил разработать удобный метод синтеза перфторированных кетонов. [23]
При использовании в реакции эпоксидирования больших концентраций катализатора ( см. табл. 2) наряду с увеличением скорости целевой реакции увеличивается количество продуктов побочных реакций гидропероксида кумола. В работах [2, 3] было показано, что с увеличением количества катализатора возрастает каталитический распад гидропероксида кумола, при этом - 30 % от неселективного распада гидропероксида расходуется на окисление спирта. [24]
Определена энергия активации реакции эпоксидирования, которая составила 69 9 кДж / моль. [25]
Изучена формальная кинетика реакции эпоксидирования 4 - ВЦГ ГПТБ в присутствии тетрабутоксититана. Порядок реакции по каждому компоненту близок к единице. Определена энергия активации, которая составила 69 9 кДж / моль. [26]
Следует отметить избирательность реакции эпоксидирования г ис-двой-ной связи в транс-транс-цис-трненовом углеводороде I; скорость этой реакции в 6 раз больше скорости эпоксидирования каждой из двух остающихся транс-двойных связей. [27]
Следует отметить избирательность реакции эпоксидирования ной связи в транс-транс-цис-трне. [28]
Проведены кинетические исследования реакции эпоксидирования. [29]
Найдены оптимальные условия реакции эпоксидирования аллилов. Хлористый и бромистый аллилы окисляются труднее соответствующих дигалоидолефинов: 1 4-дихлор - и 1 4-дибромбутенов, что не согласуется с представлением об аддитивности влияний заместителей, находящихся при реакционном центре, на скорость процесса эпоксидирования. В данном случае уравнение Тафта, коррелирующее константы скорости реакции по индукционным константам, не выполняется. Это свидетельствует о строго симметричной атаке надкислоты на облако я-электронов двойной связи. Увеличение полярности двойной связи приводит к асимметрической атаке надкислоты на олефин и затрудняет реакцию. [30]
Страницы: 1 2 3 4