Реакция - выделение - водород
Cтраница 2
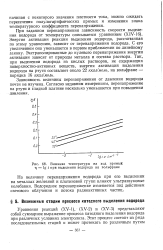 |
Влияние температуры на ход прямых т - lg i при выделении водорода на вольфраме. [16] |
Энергия активации реакции выделения водорода, рассчитанная по этому уравнению, зависит от перенапряжения водорода. С его увеличением она уменьшается в первом приближении по линейному закону. [17]
Величины & кат в реакции выделения водорода практически не зависят от природы органического донора при изменении свойств последних ( структуры, гидрофобности, окислительно-восстановительного потенциала) в достаточно широком диапазоне. [18]
В первом случае происходит реакция выделения водорода. [19]
Рассмотрим конкретный пример - реакцию выделения водорода по механизму замедленного разряда. [20]
 |
Рабочие области потенциалов оксидных электродов в диметилформамиде ( ДМФА и ацетонитриле. [21] |
Применение газодиффузионных катодов позволяет реакцию выделения водорода заменить реакцией восстановления кислорода. [22]
Так как в этих условиях реакция выделения водорода заменяется реакцией восстановления окислителя, а реакция перехода иона металла в раствор сохраняется, авторы [34] приписывали ингибитору способность тормозить лишь катодный процесс выделения водорода, отрицая его влияние на анодное растворение металла. В действительности, наблюдаемые эффекты обусловлены тем, что при введении окислителя стационарный потенциал железа сдвигается в положительную сторону и адсорбция этилхинолиниййодида - добавки катионного типа - значительно уменьшается ( рис. 1) либо может оказаться вообще невозможной. [23]
При замедленной рекомбинации для протекания реакции выделения водорода с заданной скоростью на поверхности металла необходим избыток водородных атомов по сравнению с равновесными условиями. [24]
На неоднородных поверхностях возможно протекание реакции выделения водорода по различным механизмам на разных участках поверхности. [25]
При замедленной рекомбинации для протекания реакции выделения водорода с заданной скоростью на поверхности металла необходим избыток водородных атомов по сравнению с равновесными условиями. [26]
Эти соединения почти полностью подавляют реакцию выделения водорода и заметно повышают селективность процесса. При сочетании этих двух факторов ( добавление четвертичных солей аммония в присутствии апротонных растворителей34 - 35 37 - 48 - 49) получен наиболее высокий выход адиподинитрила. Правильный выбор соотношения компонентов смеси ( акрилонитрил, четвертичная соль аммония, апротонный растворитель и донор протонов) определяет выход продукта. В качестве апротонных растворителей можно использовать органические соединения различных классов; наиболее часто48 52 рекомендуется применять ацетонитрил. [27]
Оно было получено опытным путем для реакции выделения водорода на различных металлах. Физический смысл коэффициентов а и Ъ раскрывается основной теорией кинетики электродных процессов - теорией замедленного разряда - ионизации, рассматриваемой далее ( см, гл. [28]
Оно было получено опытным путем для реакции выделения водорода на различных металлах. Коэффициент а для этой реакции зависит от природы металла в отличие от величины коэффициента Ь, которая близка к 0 12, Физический смысл коэффициентов а и b раскрывается основной теорией кинетики электродных процессов - теорией замедленного разряда - ионизации, рассматриваемой далее ( см, гл. [29]
Исследования на монокристаллах металлов подтверждают за-зисимость реакции выделения водорода от параметров эешетки. [30]
Страницы: 1 2 3 4