Реакция - катодное выделение - водород
Cтраница 2
Водородное перенапряжение зависит также от плотности тока, при котором происходит реакция катодного выделения водорода. [16]
 |
Зависимость электродного потенциала Е от от КС для КД ( 1, СД ( 2, КАС ( 3 и ингибитора Реакор-1 ( 4. [17] |
Исходя из теории замедленной электрохимической десорбции, экспериментальными критериями оценки механизма реакции катодного выделения водорода принимали величины производных ЭЕк / 9рНи дЦа / дрН, которые характеризуют зависимость кинетических параметров катодного процесса от рН среды. [18]
С учетом приведенных выше данных о влиянии ингибиторов на кинетические характеристики реакции катодного выделения водорода можно полагать, что ингибиторы блокировочного типа не меняют механизма реакции, а только уменьшают долю поверхности электрода, на которой протекает реакция. БД, как представитель таких ингибиторов, вероятнее всего адсорбируется на железе с участием я-электро-нов. Наоборот, катионоактивные ингибиторы, вызывая появление ifi - потенциала положительного знака, создают дополнительный энергетический барьер при подходе Н - ИОНОБ к поверхности электрода, что приводит к замедлению стадии разряда, которая становится лимитирующей. Ингибиторы, в ходе адсорбции которых образуются поверхностно-активные анионы, вызывают появление - потенциала отрицательного знака, ускоряя по этой причине стадию разряда и повышая, тем самым, вероятность усиления контроля катодного выделения водорода на стадии рекомбинации. Общее торможение процесса можно отнести за счет блокировки, а возможно и некоторых других эффектов, усиливающих ингибирующее действие добавки, адсорбция которой носит характер специфического или хемосорбционного взаимодействия. [19]
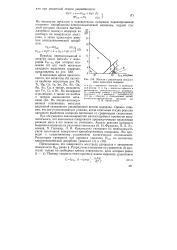 |
Области с различными механизмами выделения водорода. [20] |
Однако отметим, что могут реализоваться условия, когда отдельные стадии реакции катодного выделения водорода протекают со сравнимыми скоростями. [21]
Исследованные до настоящего времени углеродные материалы характеризуются относительно низкой электрокаталитической активностью в реакции катодного выделения водорода. [22]
В других случаях, наоборот, некоторые вещества действуют как переносчики протонов для реакции катодного выделения водорода. Так, в присутствии органических соединений, содержащих - SH-группу, эта реакция на ртутном электроде сильно ускоряется - так называемый процесс каталитического выделения водорода на ртути. [23]
Уравнение ( XII 1 - 91) было впервые выведено Фрумкиным применительно к реакции катодного выделения водорода, а затем распространено и на другие электродные процессы; оно называется уравнением Фрумкина. Это уравнение наиболее полно выражает теорию замедленного разряда и включает в себя в качестве частного случая уравнение Фольмера. [24]
Формулы (17.14) и (17.15) отвечают уравнениям Эрдей-Груза и Фольмера, выведенным применительно к реакциям катодного выделения водорода. [25]
Уравнения ( 594) и ( 595) были впервые выведены Фрумкиным применительно к реакции катодного выделения водорода, а затем распространены и на другие электродные процессы; они называются уравнениями Фрумкина. Эти уравнения наиболее полно выражают теорию замедленного разряда и включают в себя в качестве частного случая уравнения Фольмера. [26]
Формула ( XVI-44) и ( XVI-15) отвечают уравнениям Эрдей - Груза и Фольмера, выведенным применительно к реакциям катодного выделения водорода. [27]
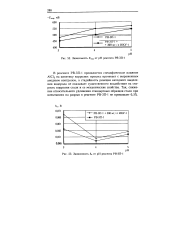 |
Зависимость Екор от рН реагента РВ-ЗП-1.| Зависимость Ьк от рН реагента РВ-ЗП-1. [28] |
В реагенте РВ-ЗП-1 проявляется специфическое влияние А1С13 на кинетику коррозии: процесс протекает с выраженным анодным контролем, а стадийность реакции катодного выделения водорода не оказывает существенного воздействия на скорость коррозии стали и ее механические свойства. [29]
Чем вызвано такое расхождение опытных данных разных исследователей и чем вызван тот факт, что даже для такой хорошо изученной реакции, как реакция катодного выделения водорода, до недавнего времени однозначно не был определен порядок реакции, вследствие чего не мог быть выяснен механизм этой реакции. [30]
Страницы: 1 2 3 4