Реакция - водяной газ
Cтраница 2
Целевыми продуктами процесса конверсии являются компоненты реакции водяного газа: водород и окись углерода. Однако в продуктах реакции обычно содержится также некоторое количество непрореагировавшего метана. [16]
Содержание С02 в газе определяется равновесием реакции водяного газа и зависит от температуры и количества водяного пара. [17]
Последние взаимодействуют между собой по так называемой реакции водяного газа ( СО EUO - С02 ЕЬ), которая имеет большое значение во всех процессах неполного горения. Эта реакция при высоких температурах идет настолько быстро, что водород, окись углерода, водяной пар и углекислота в продуктах горения, покидающих реакционное пространство, находятся обычно в равновесии. Этому равновесию не мешает присутствие в продуктах горения не только инертного азота, но и продуктов, не находящихся в равновесии. К таким продуктам можно отнести метан ( в небольшом количестве всегда присутствующий в продуктах неполного горения), ацетилен, этилен и твердый углерод в виде частичек сажи. [18]
Образование углеводородов сопровождается побочными реакциями: реакцией водяного газа, разложением окиси углерода, метанообразованием и окислением металла катализатора. [19]
Приведены результаты опытов по выяснению достижения равновесия реакции водяного газа при 600 - 700 С. Показано, что в этих условиях реакция водяного газа является быстрой и достигает равновесия. Чем больше парциальных давлений паров воды в системе, тем быстрее достигается равновесие реакции водяного газа. [20]
 |
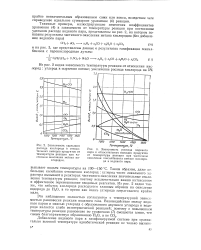
Влияние содержания метана в экзогазе иа обезуглероживание сталей различных марок. Температура иагрева 900 С, продолжительность 2 часа. [21] |
На рис. 25 приведена диаграмма равнокесня продуктов реакции водяного газа с железом. [22]
С и 927 С изменение свободной энергии реакции водяного газа проходит нулевое значение; опытом установлено, что это значение Д / 70 находится при температуре - 800 С. [23]
Как карбид, так и металл катализируют реакцию водяного газа. Не содержащие карбида катализаторы, однако, лучше действовали в реакции превращения водяного газа в углекислоту и водород. Кобальтовые катализаторы, на которых при нормальных условиях 99 % кислорода прореагировавшей окиси углерода превращаются в воду ( 180, Н2: СО 2: 1, объемная скорость 100), при изменении условий синтеза могут изменить характер своего поведения в отношении образования воды и углекислоты на противоположный. Это обусловлено протеканием реакции между первоначально образовавшейся водой и избытком окиси углерода. [24]
Реакции, вызывающие быстрое достижение равно весия в реакции водяного газа, должны тормозить ско-ро сть газификации углерода восстановлением концентрации хемосорбированного кислорода на поверхности углерода. Однако Гэдсби и соавторы [53] нашли, что добавление окиси углерода не тормозит газификацию углерода парами воды, исключая случай производства большого количества водорода, когда она действительно препятствует реакции. [25]
Эти наблюдения полностью согласуются с температурной зависимостью равновесия реакции водяного газа. [27]
Помимо того что эти процессы вызывают быстрое достижение равновесия в реакции водяного газа, они должны тормозить скорость газификации угля благодаря уменьшению концентрации хемосорбированного кислорода на его поверхности. [28]
О Реакция риформинга -) Температура 1100 - 1200 К; Реакция водяного газа. [29]
В ходе взаимодействия продуктов, не находящихся в равновесии с компонентами реакции водяного газа, состав его изменяется, так как углекислота и водяной пар превращаются в окись углерода и водород. Кроме того, температура продуктов реакции может изменяться как в результате протекания рассматриваемых эндотермических реакций, так и вследствие теплоотдачи в окружающую среду. Но ввиду быстрого установления равновесия реакции водяного газа по сравнению с другими одновременно протекающими реакциями можно считать, что ( при температурах выше 1000) это равновесие в каждый момент времени соответствует температуре процесса. [30]
Страницы: 1 2 3 4