Реакция - водяной газ
Cтраница 3
В восстановлении Na2S04 возможно также участие во рода, образующегося как по реакции водяного газа, так и i диссоциации углеводородов, которые могут присутствовав углеродсодержащих газообразователях. [32]
В последних работах Крэксфорд [52] принимает, что двуокись углерода образуется по реакции водяного газа, а метан и газообразные углеводороды образуются в результате гидрокрекинга. [33]
Равновесный состав продуктов сгорания не зависит от давления, так как, реакция водяного газа происходит без изменения числа молей. Поэтому константа равновесия этой реакции зависит только от температуры. [34]
Оно будет одним и тем же, независимо от конкретного пути протекания реакции водяного газа. [35]
Данные табл. 6 показывают, что в газе практически устанавливается термодинамическое равновесие реакции водяного газа. [36]
 |
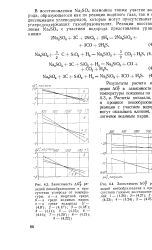
Равновесные условия реакции дегидрирования н-бутиленов. [37] |
Главным источником потерь являются реакции расщепления, в частности каталитический крекинг дивинила и реакция водяного газа с образованием двуокиси углерода. Важное значение для выходов имеет также реакция каталитической полимеризации дивинила и распада димера. [38]
Присутствие окиси калия ускоряет взаимодействие между водой и углеродом с образованием СО2 ( реакция водяного газа), благодаря чему некоторые катализаторы дегидрирования этилбензола с применением водяного пара становятся саморегенерирующимися, что делает процесс контактирования этилбензола непрерывным. [39]
Главным источником потерь являются реакции расщепления, в частности каталитический крекинг бутадиена и реакция водяного газа с образованием двуокиси углерода. Важное значение для выходов имеют также реакции каталитической полимеризации бутадиена и распада димера. [40]
Влияние окиси хрома на активность окиси железа; уменьшение активности окиси железа в реакции водяного газа выше 800 очень быстрое, оно может быть предотвращено добавлением 7 мол. [41]
Следовательно, в работающем двигателе идеальная закалка состава реакционной смеси, соответствующего равновесию реакции водяного газа при температуре взрыва, не имеет места. Это обусловлено тем, что в момент взрыва в цилиндрах двигателя температура превышает 2000 и благодаря этому в начале последующего такта рабочий ход скорость смещения равновесия в объеме достигает заметной величины. Дальнейшее резкое падение температуры реакционной смеси в течение такта рабочий ход сопровождается снижением скорости смещения равновесия, в результате чего конечный состав реакционной смеси должен соответствовать равновесию реакции водяного газа при определенной температуре, про межуточной между температурами взрыва и выхлопа. [42]
Получение безокислительной атмосферы возможно путем расчета ее состава, руководствуясь кривой равновесия продуктов реакции водяного газа с железом, приведенной на фиг. [43]
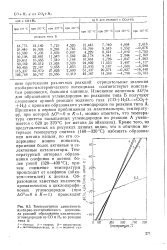 |
Температурная зависимость изобарно-изотермического потенциала реакций образования циклических углеводородов из СО и Н2 по реакции типа А. [44] |
Изменение величины AG / для образования углеводородов по реакциям типа Б получают сложением кривой реакции водяного газа ( СО О - - СС2 Н2) с кривыми образования углеводородов по реакции типа А. Кроме того, из представленных на рисунках данных видно, что в обычном интервале температур синтеза ( 160 - 320 С) избежать образования метана нельзя, но его содержание можно понизить, применяя более активные и селективные катализаторы. Температурный интервал образования олефинов и диенов более узкий ( 320 - 400 С), причем снижение температуры происходит от олефинов ( эйко-зен-иэтилен) к диенам. [45]
Страницы: 1 2 3 4