Реакция - гидродеалкилирование
Cтраница 2
Показана [87] высокая эффективность в реакции гидродеалкилирования толуола декатионированных цеолитов типа X и Y, активированных металлами VI и VIII групп периодической системы элементов. Выявлено, что в цеолите эффективный размер входных пор должен быть больше 6 6 А, достаточный для свободного доступа молекул бензола и алкилбензолов к активным центрам и отвода продуктов реакции. Мала активность низкокремнеземного цеолита типа А объяснялась тем, что максимальный диаметр его окон составлял 5 А. [16]
Цеолит 0 5PdHY использовали в реакции гидродеалкилирования алкилароматических углеводородов тяжелой бензиновой фракции ( 170 - 250 С), содержавшей 75 объемн. В процессе при 260 - 329 С параллельно протекали две реакции - крекинг и деалкилирование. [17]
В других работах [53] порядок реакции гидродеалкилирования ксилолов также был найден равным 1 5; этот порядок принят и для многих аналогичных реакций. [18]
Была проверена [31] пригодность многочисленных Катализаторов реакции гидродеалкилирования. [19]
Дж / моль) затрудняет осуществление реакции гидродеалкилирования. [20]
Влияние давления на выход нафталина при реакциях гидродеалкилирования, вероятно, зависит от многих факторов. Одним из них, очевидно, является активность катализатора при гидрировании нафталинов до тетра-линов и декалинов. После образования этих гидроароматических углеводородов они крекируются примерно с такими же скоростями, как неароматические. [21]
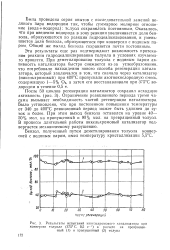 |
Результаты испытаний никельхромового катализатора при конверсии толуола ( 375 С, 0 5 ч. - 1 в расчете на превращенный ( / и пропущенный ( 2 толуол. [22] |
Эти результаты еще раз подтверждают возможность протекания реакции гидродеалкилирования толуола в условиях изучаемого процесса. [23]
В табл. 1 - 3 приведены значения теплот реакций гидродеалкилирования, приводящих к образованию метана, этана или пропана и соответствующего ароматического углеводорода. [24]
Во всех этих институтах разрабатываются процессы, основанные на реакции гидродеалкилирования. [25]
Наиболее полно и достаточно селективно ( свыше 95 %) реакции гидродеалкилирования протекают в присутствии окисных катализаторов, содержащих молибден, кобальт, хром на окиси алюминия. Для предотвращения коксообразования, протекающего преимущественно на кислотных активных центрах, в катализатор вводят соединения щелочных металлов или воду. [26]
В соответствии с законами термодинамики давление не должно оказывать влияния на равновесие реакции гидродеалкилирования. Однако в связи с кинетическими особенностями протекания реакции процессы гидродеалкилирования в промышленных масштабах обычно проводят под давлением 50 - 70 ат в присутствии катализаторов или без них при 650 - 750 С. [27]
 |
Константы равновесия реакций гидродеалкилирования метилпроизводных ароматических углеводородов. [28] |
В соответствии с законами термодинамики, давление не должно оказывать влияния на равновесие реакции гидродеалкилирования. Однако в связи с кинетическими особенностями протекания реакции процессы гидродеалкилирования в промышленных масштабах обычно проводят под давлением 5 0 - 7 0 МПа ( 50 - 70 кгс / см2) в присутствии: катализаторов или без них при 600 - 750 С. [29]
Кажущаяся энергия активации в предположении 1 5-порядка является фактически суммой истинной энергии активации реакции гидродеалкилирования и величины, выражающей температурную зависимость константы равновесия для реакции диссоциации водорода. В этом смысле полученная величина представляет собой энергию псевдоактивации. Хотя этот показатель исключительно важен для практических расчетных целей, возникают некоторые сомнения относительно того, насколько величина его отражает механизм протекающих реакций. [30]
Страницы: 1 2 3 4