Реакция - кислотный гидролиз
Cтраница 1
Реакции кислотного гидролиза играют значительную роль в так называемых процессах предварительной обработки ( например, при ацетилировании) и в реакциях собственно замещения. Протеканием реакций гидролиза объясняется химическая неустойчивость сложных эфиров целлюлозы по отношению к остаточным кислотам ( серной, азотной) или к кислотам, образующимся вследствие омыления самих эфирных групп. Стабилизация литратов и ацетатов целлюлозы состоит поэтому в полном удалении этих примесей, во введении в полимеры солей, способных нейтрализовать их по мере образования, или в нейтрализации кислотных заместителей ( - OSO3H) с превращением их в стабильные негидролизующиеся продукты. [1]
Поскольку реакции кислотного гидролиза комплексов Со ( Ш) типа упомянутых выше, как правило, медленные, то кажется очевидным, что эта реакция бикарбонато-комплекса может происходить по совершенно иному механизму. [2]
Были изучены реакции кислотного гидролиза, основного гидролиза, реакции замещения галогенами в кислых средах. Механизм реакций довольно сложен. [3]
Определение основано на реакции кислотного гидролиза. [4]
Наряду с ферментативной деструкцией реакция кислотного гидролиза является наиболее важной и типичной реакцией деструкции гликозидов, дисахаридов, олигосахаридов и полисахаридов. Гидролиз полисахаридов древесины - целлюлозы и полиоз - проводят в технических процессах и при анализе древесины. [5]
Аналогичные пространственные эффекты проявляются при реакции кислотного гидролиза сложных эфиров, протекающей по тримолекулярному механизму, а также при реакции их омыления щелочами. В частности, устойчивость сложных эфиров ди-алкилмалоновых ( I) и татраалкилянтарных ( II) кислотно отношению к гидролизу также объясняется влиянием пространственных факторов. [6]
После удаления сульфогрупп из продукта реакции путем кислотного гидролиза получены почти в равных количествах о-цимол и 2 6-диизопро-пилтолуол. [7]
Остается так же непонятным, почему в реакции кислотного гидролиза орго-замещенных алкилбензоатов стерический эффект отсутствует [ 37, с. [8]
Какой из изомерных диаминонафталинов легче вступает в реакцию кислотного гидролиза. [9]
Какой из изомерных диаминонафталинов легче вступает в реакцию кислотного гидролиза. [10]
В качестве таковой оказалось удобным предложить [61] реакцию кислотного гидролиза эфиров карбоновых кислот. Эта реакция крайне нечувствительна к индукционным эффектам заместителей, что выражается в очень низких значениях реакционной константы р, варьирующих в пределах от - 0.2 до - j - 0.5 в зависимости от условий ее проведения. Показательно, что и в ароматическом ряду кислотный гидролиз м - и - замещенных бензоатов, как и кислотная этерификация, также вполне индифферентен к действию электронных эффектов заместителей, хотя здесь кроме / - эффекта включаются еще М - и С-влияния. [11]
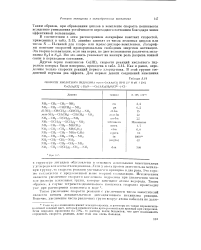 |
СКОРОСТИ КИСЛОТНОГО ГИДРОЛИЗА транс - Со ( АА2 С1. ПРИ 25 И рН 1. [12] |
Другая серия комплексов Со ( Ш), скорости реакций кислотного гидролиза которых были измерены, приведена в табл. 3.14. Как и ранее, определены только скорости реакций первого хлорид-иона. В этой группе соединений изучены два эффекта. [13]
Таким образом, эта реакция декарбоксилации происходит быстрее, чем реакция кислотного гидролиза. [14]
 |
Сложные эфиры гомологов муравьиной кислоты. [15] |
Страницы: 1 2 3