Реакция - кислотный гидролиз
Cтраница 2
Механизм этой реакции, очевидно, тот же, что и реакции кислотного гидролиза. [16]
Тафтом показано, что величины ES е являются специфическими стерическими характеристиками заместителей только в реакции кислотного гидролиза сложных эфиров. [17]
Поэтому было высказано предположение, что циклотриэфиры типа II не являются истинными промежуточными продуктами в реакции кислотного гидролиза, а существуют лишь в виде активированного комплекса типа Па, протонированного по кислороду гидроксиль-ной группы при С-2 ( или С-3) остатка рибозы 36 ( о протонирова-нии этих групп в процессе кислотного гидролиза нуклеозид-2 3 -циклофосфатов см. стр. [18]
 |
Механизм катализируемого кислотами и основаниями включения 18О в карбонильные соединения. О обозначает 1вО, а - 180. [19] |
Пользуясь механизмом, данным на рис. 17 - 2 в качестве модели, напишите механизмы реакций кислотного гидролиза перечисленных ниже альдиминов и кетиминов, в результате которых образуются соответственно альдегиды и кетоны. [20]
Такое предположение соответствует наблюдаемым различиям в характере влияния электронодонорных и электроноакцепторных заместителей на кинетические параметры реакции кислотного гидролиза пиримидиновых дезоксинуклеозидов. [21]
Из табл. 2 видно, что чем больше константа диссоциации амина, тем больше константа скорости реакции кислотного гидролиза соответствующего бензального его производного. [22]
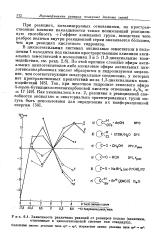 |
Зависимость различных реакций от размеров кольца ( величины, отнесенные к циклогексановой системе как стандарту. [23] |
При реакциях, катализируемых основаниями, на пространственные влияния накладывается также понижающий реакционную способность / - эффект алкильных групп, вследствие чего разброс величин внутри реакционной серии оказывается большим, чем при реакциях кислотного гидролиза. [24]
Стеклообразующие оксиды кремния и титана вводят из соединений, склонных к гидролизу-ортозтилсиликата и ортозтилтитана. Реакция кислотного гидролиза ортоэтилсиликата [ этилового эфира ортокремниевой кислоты тетраэтоксисилана HaO Si ] состоит из ряда стадий, зависящих от количества участвующей в гидролизе воды и приводящих к образованию поликремниевых эфиров. [25]
Метод основан на реакциях кислотного гидролиза, последующего окисления перманганатом калия или хромовой кислотой для образования альдегидных групп в полисахарной цепи и взаимодействия с карбонатом серебра. [26]
Выше уже рассматривался вопрос о причинах, вызывающих десульфирование растворимых сульфокислот фенолов и полиметиленполпфенолов при проведении их конденсации с формальдегидом в кислой среде. Определенное значение здесь имеет реакция непосредственного кислотного гидролиза фенолсульфокислот. При этом, однако, следует учесть, что / г-фенолсульфокислота. [27]
Образец жира может вступить ( при определенных условиях) в реакцию с 0 05 моль водорода. Продукт гидрирования вступает в реакцию кислотного гидролиза. [28]
Хотя замещение координированного хлора в метаноле прямо приводит к потере оптического вращения, его замещение в водных растворах в значительной степени проходит с сохранением конфигурации. Поскольку полагают, что как реакция кислотного гидролиза в водных растворах, так и обмен хлором в метаноле идут по межмолекулярному механизму с участием растворителя внешней сферы, очевидно, что скорость исчезновения сольвато-комплекса не должна быть одинаковой. Это различие может быть объяснено тем, что донорная способность воды выше донорной способности метанола. [29]
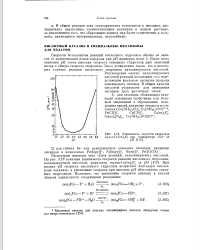 |
Зависимость скорости гидролиза. [30] |
Страницы: 1 2 3