Реакция - алкилирование - фенол
Cтраница 3
Для получения чистого изобутилена можно использовать способность третичного углеродного атома легко вступать в реакцию алкилирования фенола и затем легко отщепляться. [31]
Для установления количественных зависимостей между составом алкилата, константами скорости и скоростью реакции изучена кинетика реакции алкилирования фенола пропиленом в присутствии хлористого алюминия. [32]
Для получения стабилизатора п ароматическое кольцо вводят а л кильн ые группы, разветвленные на а-агоме углерода; наибольшее практическое значение имеют реакции алкилирования фенолов олсфинами к циклоолефинами в присутствии кислотных катализаторов. [33]
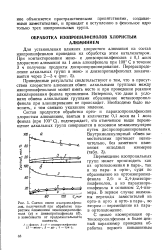 |
Состав смеси изопропилфенолов, полученный при обработке хлористым алюминием моноизопропилфе-нола ( а и диизопропилфенола ( б, в зависимости от продолжительности контакта. [34] |
Приведенные результаты свидетельствуют о том, что в присутствии хлористого алюминия обмен алкильными группами между изопропилфенолами может иметь место и при проведении реакции алкилирования фенола пропиленом. Интересно, что даже в условиях обмена алкильными группами образование метаизопропил-фенола при алкилировании не происходит. Необходимо было выяснить, с чем связано указанное явление. [35]
Уменьшение молекулярной массы полиизобутилена и количества связанного фенола с повышением температуры полимеризации отражает неблагоприятное влияние смещения равновесия ионы ионные пары вправо как на стадии роста, так и на стадии сопряженной с ней реакции алкилирования фенола - ограничения цепи. Содержание фракции полиизобутилена с концевыми фенольными группами мало зависит от молекулярной массы полимера для фракционированных образцов [245], что также согласуется с сосуществованием реакций роста и обрыва цепи в результате сопряженного алкилирования. [36]
Более подробно вопрос алкилирования фенолов спиртами не рассматривался, так как в промышленности эти процессы по экономическим соображениям имеют ограниченные перспективы применения и подчиняются тем же закономерностям, что и алкили-рование фенолов олефинами. Исключение составляют реакции алкилирования фенолов метиловым спиртом, которым в последнее время уделяется большое внимание. Они позволяют получать ряд весьма дефицитных в народном хозяйстве метилфенолов, которые другим способом не могут быть получены. [37]
Литературные данные и наши систематические исследования в этой области показывают, что наиболее простым, интересным и перспективным синтезом алкилфенолов и их алкиловых эфиров, как и описанных в гл. II алкилбензолов, является реакция алкилирования фенолов и алкилфенило-пых эфиров олефинами. Что же касается алкилирования спиртами, галоидными алкилами и эфирами, то, по нашему мнению, оно пе является перспективным для промышленного развития, так как не обеспечивается доступным сырьем ( указанные алкилирующие агенты, как правило, получаются на основе олефипов) и не имеет каких-либо преимуществ по сравнению с алкилированием олефипами в смысле организации производства, его простоты и выходов продуктов. [38]
Теперь для этой реакции применяются очень многие катализаторы. Приблизительно до 1935 г. реакция алкилирования фенолов олефинами представляла главным образом научный интерес. За последние 20 - 25 лет в связи с интенсивным развитием нефтеперерабатывающей промышленности, в особенности процессов крекинга и пиролиза, поставляющей поистине неограниченные количества олефинов, она приобрела важное практическое значение и широко внедряется в промышленность. [39]
Теперь для этой реакции применяются очень многие катализаторы. Приблизительно до 1935 г. реакция алкилирования фенолов олефинами представляла главным образом научный интерес. За последние 20 - 25 лет в связи с интенсивным развитием нефтеперерабатывающей промышленности, в особенности процессов крекинга и пиролиза, поставляющей поистине неограниченные количества олефинов она приобрела важное практическое значение и широко внедряется в промышленность. [40]
Интересно отметить, что в отличие от реакции алкилирования фенолов оле-финами, когда при перегонке продуктов реакции приходится отбирать 4 - 5 фракций, в данном случае эфирный продукт почти полностью перегоняется при 145 - 146 / 12 мм и представляет чистое индивидуальное вещество с хорошими данными анализа. [41]
Объектом исследования служил газовый бензин сланцеперерабатывающего комбината в г. Кохтла-Ярве. С целью использования газбензина для химической переработки исследована реакция алкилирования фенола углеводородами газбензина в присутствии различных кислотных катализаторов. [42]
Алкилирование фенолов в присутствии фтористого бора было изучено А. В. Топчиевым, С. В. Завгородним, Я. М. Паушкиным, М. В. Кураше-вым [32] и другими исследователями. Новым катализатором для алкилирования фенола является алюмосиликат, который для этой цели впервые был изучен А. В. Топчиевым, Я. М. Паушкиным и М. В. Курашевым [32] в 1959 - 1960 гг. Реакция алкилирования фенола на алюмосиликате проводится при 100 - 160 С, но оптимальной температурой является 130 С. При алкилировании фенола на алюмосиликате при молярном соотношении реагентов 1: 1 в алкилате остается 13 - 15 % свободного фенола и образуется 85 - 87 % алкилфенолов. [43]
Фенолы легче алкилируются, чем ароматические углеводороды. Однако и здесь с успехом применяют катализаторы Фриделя-Крафтса, например безводный хлористый алюминий, хлористый цинк, хлорное железо и др. Даже относительно небольшие количества серной кислоты также катализируют реакцию алкилирования фенолов. [44]
Наиболее интересным с точки зрения простоты выполнения, а также доступности исходных веществ является алкилирова-ние фенола олефинами. Процесс протекает в присутствии катализаторов, которыми в преобладающем большинстве случаев являются сильные кислоты или другие вещества кислотного характера. Одним из первых катализаторов, нашедших применение в реакции алкилирования фенола олефинами, так же как и при алкилировании спиртами, является серная кислота. Оптимальное количество концентрированной кислоты как катализатора этого процесса составляет 8 - 10 % от веса фенола. [45]
Страницы: 1 2 3 4