Реакция - деалкилирование
Cтраница 1
Реакция деалкилирования получает заметное развитие при 130 С и выше. [1]
Реакция деалкилирования в отличие от о-крезола практически не протекает с ж-крезолом, а с л-крезолом идет лишь при 400 С. При этой температуре л-крезол деалкилируется в 1 85 раза медленнее орто-изомера. [2]
Реакция деалкилирования галоидными солями одноименных металлов, столь четко протекающая у оловоорганических соединений, в случае германийорганических соединений проходит более сложно, приводя к смеси продуктов различной степени алкилирования, причем второй радикал отщепляется только в присутствии катализатора. У свинцовоорганических соединений реакции этого типа остаются мало изученными. [3]
Реакция деалкилирования с помощью GeX4, так широко применяемая в ряду оловоорганических соединений, для германийорганических соединений идет труднее. Реакция требует применения катализаторов - хлористого алюминия или алюминийорганических соединений. Соединения типа RGeX3 методом деалкилирования получаются плохо, их лучше синтезировать другими способами, например прямым методом. [4]
Реакции деалкилирования и деарилирования ( описанные в гл. IX) приводят к разрыву бор - углеродных связей. [5]
Реакции деалкилирования и деарилирования висмуторганических соединений типа R3Bi изучены в основном с точки зрения исследования прочности связи висмута с углеродом по отношению к различным реагентам. Для применения этих реакций в синтетических целях требуются, вероятно, дополнительные исследования. Реакции с кислотами, фенолами и тиофенолами проводились в жестких условиях, при которых происходит исчерпывающее деарилирование висмут-органического соединения. При применении эквимолекулярных количеств реагентов образуются соединения типа ArBiX2, но большая часть триарил-висмута остается при этом без изменения. Исчерпывающее деарилирование висмуторганических соединений наблюдается, как правило, и при проведении реакций с солями металлов. [6]
Реакция деалкилирования была выбрана не случайно. [7]
Реакции деалкилирования, дегидрирования, распад кольца, характерные для крекинга нафтенов, ускоряются в присутствии катализатора в 500 - 4000 раз. Дегидрирование и деалкилирование нафтенов протекают с перераспределением водорода. В результате накапливаются ароматические и парафиновые углеводороды. [8]
Реакция деалкилирования идет гладко по связи Сар - Сал. [9]
С реакция деалкилирования проходит до трехбромистой сурьмы. [10]
Протеканию реакций деалкилирования способствуют высокая температура и низкая объемная скорость подачи сырья. Скорость деалкилирования резко увеличивается с возрастанием числа углеродных атомов в молекулах исходных углеводородов. Однако скорости этих реакций самые низкие по сравнению с другими основными реакциями риформинга. [11]
Механизм реакции деалкилирования не изучен. [12]
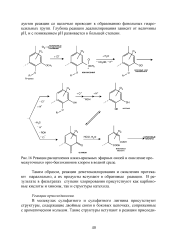 |
Реакции расщепления алкил-арильных эфирных связей и окисление про-межуточныхо орто-бензохинонов хлором в водной среде. [13] |
Глубина реакции деалкилирования зависит от величины рН, и с понижением рН развивается в большей степени. [14]
Скорость реакции деалкилирования кумола описывается уравнением тормозящихся мопомолекулярных реакций во всем интервале степеней его превращения. Это объясняется, невидимому, тем, что в этом случае при переходе от малых к большим объемным скоростям характер превращения кумола заметно не меняется. [15]
Страницы: 1 2 3 4