Любая реакция
Cтраница 4
В любой реакции, где изменение свободной энергии не вызывает противоположного изменения энтропии, изменение энтальпии будет более значительным, чем изменение только свободной энергии. [46]
Скорость любой реакции зависит от числа эффективных столкновений активированных молекул с обычными, а вероятность соударений - от длительности активации та и концентрации молекул. [47]
Скорость любой реакции зависит от числа эффективных столкновений активированных молекул с обычными. Вероятность таких соударений, в свою очередь, зависит от длительности активации ( - - средняя продолжительность существования активированных молекул) и концентрации. [48]
Для любых реакций следует иметь в виду, что при некоторой температуре ( так называемой изокинетической) последовательность влияния заместителей на скорость или равновесие реакции может измениться на противоположную, без изменения механизма реакции; чем ближе используемая температура к изокинетической, тем слабее влияние заместителей Поэтому для строгого доказательства характера реагентов по влиянию заместителей необходимо знание изокинетической температуры ( см. L e f f 1 е г, J. [49]
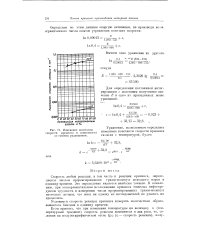 |
Изменение константы 1. [50] |
Скорость любой реакции, в том числе и реакции крекинга, определяется числом прореагировавших грамм-молекул исходного сырья в. Это определение является наиболее точным. К сожалению, при экспериментальном исследовании крекинга тяжелых нефтепродуктов трудности в измерении числа прореагировавших грамм-молекул настолько велики, что пока ни одному из исследователей не удалось их преодолеть. [51]
Скорость любой реакции зависит от числа эффективных столкновений активированных молекул с обычными. Вероятность таких соударений, в свою очередь, зависит от длительности активации ( т-средняя продолжительность существования активированных молекул) и концентрации. [52]
Для любой реакции можно различать по крайней мере три величины AS, представляющие интерес: Д5всел, Д окруж и Д5СИСТ, В большинстве случаев указывается величина Д5СИСТ, так что, если величина AS приведена без индекса, то подразумевается, что она относится к рассматриваемой системе. В большинстве случаев в этом курсе рассматриваются системы, в которых происходят химические реакции. Такие химические системы обычно состоят из реагентов и продуктов, указанных в уравнении реакции. [53]
Страницы: 1 2 3 4