Внутримолекулярная реакция
Cтраница 2
Внутримолекулярная реакция Вильямсона ( вызываемая основанием циклизация галогеноспиртов) - стандартный способ получения оксиранов, оксетанов и высших циклических простых эфи-ров ( см. разд. [16]
Внутримолекулярные реакции сочетания, которые используются для получения цинполинов или индазолов, проводятся н сильнокислом растворе. Это способствует протеканию реакции сочетания и уменьшает происходящее одновременно разложение соли диазонин с образованием фенола. По тем же причинам применяют кислые растворы в случае реакций солей диазония с углеводородами. [17]
Внутримолекулярные реакции внедрения гораздо более селективны, так как здесь определяющую роль в распределении продуктов реакции играет относительная: близость различных связей С -: Н к карбеновому центру. Поэтому такие реакции находят синтетическое применение н особенно ценны при синтезе производных сильно напряженных циклических систем. [18]
 |
Конформация открытой углеродной цепи. [19] |
Внутримолекулярные реакции образования циклических ангидридов, эфиров, амидов и других производных распространены довольно широко, что связано с выгодностью образования термодинамически устойчивых пяти - и шестичленных циклов. [20]
Внутримолекулярные реакции арилацетиленов привлекли вни мание в последние годы. Диэтинилбифенил реагирует с бромистым водородом, образуя 9 Ю - бис ( бромметил) фенантрен. [21]
Внутримолекулярные реакции ацилирования арилзамещенных кислот жирного ряда были широко изучены Физером. Эти исследования охватили производные бензола, аценафтена, дифенила, фенантрена, пирена, ретена, нафталина и бензантрацена. Методика проведения реакций была аналогична описанной выше. [22]
Внутримолекулярными реакциями [2 2] циклоприсоедннения получен ряд очень интересных каркасных соединений, например, производных кубана. [23]
Внутримолекулярными реакциями замещения, протекающими при участии соседней группы, очень широко пользуются в тех случаях, когда нужно произвести определенные стереохимические изменения в молекуле. Уинштейн и Бошан [1] в своем обзоре рассмотрели использование в такого рода реакциях сложных заместителей, находящихся по соседству с группой, конфигурацию которой надо обратить. Описано [2] применение фснилтиокарбамоильной группы для этой цели в ряду производных циклогексана. В данной статье описано получение анилиносахара в результате внутримолекулярной реакции замещения соучаствующей соседней фенилтиокарбамоильной группой. Проблема общности этого типа инверсии применительно к другим замещенным тиокарбамоильным группам и другим сахарам остается нерешенной и требует дополнительных исследований. [24]
Это внутримолекулярная реакция, протекающая в газовой фазе без побочных процессов, нечувствительна к действию внешних катализаторов и подчиняется кинетике первого порядка. [25]
Эта внутримолекулярная реакция напоминает электрофильное замещение, происходящее в активированном фенольном цикле. [26]
Эти внутримолекулярные реакции удалось проследить благодаря тому, что в синтетических нуклеотидо - ( Р - М) - аминокислотах гидро-ксильная группа, расположенная по соседству с нуклеотидолептидным фосфором, была блокирована ацетильным остатком. [27]
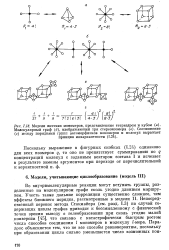 |
Модели жестких мономеров, представленные тетраэдром и кубом ( а. [28] |
Во внутримолекулярные реакции могут вступить группы, разделенные на молекулярном графе сколь угодно длинным маршрутом. Учесть такие дальние корреляции существенно сложнее, чем эффекты ближнего порядка, рассмотренные в модели II. Непосредственный перенос метода Стокмайера ( см. разд. [29]
Используя внутримолекулярные реакции, иногда удается получить полимеры нового типа, обладающие совершенно новыми свойствами по сравнению с исходными полимерами. [30]
Страницы: 1 2 3 4