Значение - критический потенциал
Cтраница 2
Никаких экспериментальных доказательств этой формулы или указаний на присутствие или отсутствие типичных для перекисей связей О-О не имеется. Неясно также, относятся ли приведенные в литературе значения критического потенциала выделения к обратимому процессу. [16]
Аноды были платиновыми с площадью 10 см2, катоды из платины, кадмия или олова имели площадь 5x2.5 см. Активность цинка, осажденного на электроде, определялась по разности начальной активности и активности, оставшейся в растворе после электролиза. Полученные кривые ( рис. 256) показывают, что значение критического потенциала близко к - 1.0 V для электродов из кадмия и олова, а для платины оно несколько выше. Значение критического потенциала, полученное из уравнения ( 85), равно - 1.18 V. [17]
Аноды были платиновыми с площадью 10 см2, катоды из платины, кадмия или олова имели площадь 5x2.5 см. Активность цинка, осажденного на электроде, определялась по разности начальной активности и активности, оставшейся в растворе после электролиза. Полученные кривые ( рис. 156) показывают, что значение критического потенциала близко к - 1.0 V для электродов из кадмия и олова, а для платины оно несколько выше. [18]
Жолио и Вертенштейн [ J22, W19 ] нашли, что изменение концентрации полония в 100 раз ( при концентрации приблизительно 10 - 10М) не вызывает изменения критического потенциала осаждения на катоде при осаждении полония на золоте из раствора разбавленной кислоты. Однако значение эксперименталь - ных погрешностей в их работе ( - 0 03 в) было столь же велико, как и значения критического потенциала, которые они пытались определить. [19]
Анодная кривая сплава Ti - 0 2 % Pd в условиях щели при 160 С характеризуется очень широкой областью пассивного состояния, а потенциал начала развития щелевой коррозии сдвинут в положительную сторону по сравнению с критическим потенциалом для Ti в щели на 1 35 В. В то же время анодные кривые Ti и сплава Ti - 0 2 % Pd в объеме раствора отличаются незначительно как по величине тока, так и по значениям критических потенциалов, хотя критический потенциал Ti - 0 2 % Pd все же тюложительнее. Эти результаты свидетельствуют о том, что меха-шизм защитного действия легированного титана сводится к накоплению палладия в условиях ограниченного объема раствора в щели и к снижению перенапряжения катодного выделения водорода. [20]
Быстрое разрушение графита при потенциалах выше критического связано с набуханием и разрывом близких к поверхности слоев. Это происходит при интенсивном выделении кислорода вследствие образования фазовых оксидов внутри кристаллической решетки графита. Значение критического потенциала ограничивает значение плотности тока на графитовом аноде и, следовательно, определяет интенсивность процесса электролиза. [21]
Аноды были платиновыми с площадью 10 см2, катоды из платины, кадмия или олова имели площадь 5x2.5 см. Активность цинка, осажденного на электроде, определялась по разности начальной активности и активности, оставшейся в растворе после электролиза. Полученные кривые ( рис. 256) показывают, что значение критического потенциала близко к - 1.0 V для электродов из кадмия и олова, а для платины оно несколько выше. Значение критического потенциала, полученное из уравнения ( 85), равно - 1.18 V. [22]
В своих исследованиях Гарди полагал, что коагуляция должна наступать в изоэлектрической точке, когда - потенциал частиц равен нулю. Существенно, что значение критического потенциала в общем оказалось мало зависящим от вида электролита, с помощью которого он был достигнут. [23]
В своих исследованиях Гарди полагал, что коагуляция должна наступать в изоэлектрической точке, когда - потенциал частиц равен нулю. Однако позднее было установлено, что коагуляция обычно наступает не в изоэлектрической точке, а при достижении некоторого критического - потенциала. Существенно, что значение критического потенциала в общем оказалось мало зависящим от вида электролита, с помощью которого он был достигнут. [24]
 |
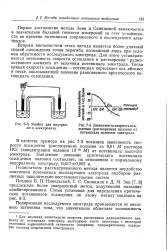
Зависимость потенциала выделения Ро от логарифма его концентрации в растворе НС1. [25] |
Использовались как внутренний, так и внешний электро-лизы с применением вышеуказанной методики. В табл. 190 приведены полученные авторами значения критических потенциалов. [26]
 |
Ячейка для внутреннего электролиза.| Зависимость скорость осаждения ( растворения полония от потенциала золотого электрода. [27] |
Вторым достоинством этого метода является более удачный способ нахождения точки перегиба, возможный лишь при условии обратимости исследуемого электрода. Для этого устанавливается зависимость скорости осаждения и растворения радиоактивного элемента от величины потенциала электрода. Тогда кривая скорость осаждения - потенциал пересекает ось абсцисс в точке, показывающей значение равновесного критического потенциала осаждения. [28]
Согласно рассматриваемой теории, степень гетерогенности поверхности должна влиять на форму кривых осаждения. Чем больше разница в энергиях адсорбции между наиболее активными и наименее активными участками поверхности, тем более растянутой должна быть кривая и тем больше должен быть ее наклон к оси абсцисс. В случае поверхности однородной в энергетическом смысле осаждение не должно происходить совершенно до достижения значения критического потенциала, но затем кривая должна подниматься почти перпендикулярно к оси абсцисс. Это действительно наблюдалось [27] для случая выделения висмута на ртути - металле, обладающем, как известно, почти идеально равной поверхностью. [29]
На сплавах с более отрицательными значениями потенциала ( от - 0 7 до - 1 0 В) питтинг практически не образовывался. Причина такого поведения сплавов становится понятной, если сопоставить указанные области коррозионных потенциалов со значением критического потенциала питтинго-образования в 3 % растворе NaCl, которое составляет - 0 45 В ( см. разд. Контакт образцов сплавов, склонных к питтингу, с пластинами активного алюминиевого сплава ( см. разд. В в основном успешно предотвращал образование питтинга в течение всего периода испытаний. Результаты этих испытаний в реальных условиях подтверждают предположение, что в отсутствие щелей алюминий и его сплавы при потенциалах ниже критического значения не подвергаются питтинговой коррозии. [30]
Страницы: 1 2 3