Индикаторная реакция
Cтраница 3
Что называют индикаторной реакцией и индикаторным веществом. Какие требования предъявляются к индикаторным реакциям. [31]
 |
Кривая каталиметрнческого титрования Ag раствором KI. Рис, 14. Кривая каталиметрического титрования 1 - раствором AgNO3. [32] |
В некоторых случаях индикаторная реакция резко ускоряется избыточной каплей раствора катализатора, что приводит к заметному изменению окраски при непосредственном титровании. [33]
В процессе изучения индикаторных реакций была проведена модификация субстратов, целью которой, с одной стороны, было подтверждение предполагаемого механизма процесса, а с другой, - поиск новых более чувствительных индикаторных реакций. Данные о механизме каталитического действия никеля и кобальта в реакциях тайрон - Н20а, дифенилкар-базон - - Н202, дифенилкарбазон - тайрон - Н202; меди в реакции гидрохинон - пиридин - Н202; хрома в реакции о-дианизидин - Н20 дали возможность предположить, что образуются промежуточные активные комплексные соединения субстрата с катализатором. [34]
 |
Индикаторные реакции для определения иридия кинетическим методом. [35] |
В табл. 3 приведены индикаторные реакции для определения иридия кинетическим методом. [36]
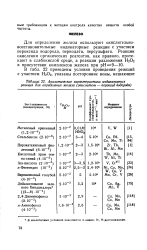 |
Аналитические характеристики индикаторных реакций для определения железа ( окислитель - пероксид водорода. [37] |
Для определения железа используют окислительно-восстановительные индикаторные реакции с участием пероксида водорода, периодата, персульфата. [38]
Высокой чувствительностью обладают и другие индикаторные реакции с перекисью водорода в качестве окислителя. Например, в присутствии катализаторов она окисляет некоторые органические красители, что сопровождается появлением или исчезновением яркой окраски растворов. Скорость таких реакций измеряется по изменению светопо-глощения растворов в единицу времени. К достоинствам реакций можно отнести и то, что для некоторых красителей они специфичны: окисление Н - кислоты, сложного органического красителя, катализируется только соединениями железа, а окисление другого органического красителя - тропеолина 00 - катализируется только соединениями шестивалентного хрома. В табл. 6 указаны пределы концентрации катализаторов, определяемой с помощью реакций окисления перекисью водорода органических красителей. При помощи таких реакций окисления определяют железо, медь и хром в веществах особой чистоты и в некоторых солях редкоземельных элементов. [39]
В табл. 2 приведены основные индикаторные реакции для определения рутения кинетическим методом. [40]
Важное значение имеет скорость индикаторной реакции. Способ измерения этой скорости должен быть простым, удобным и быстрым. Наиболее удобно измерять скорость реакции по концентрации исходного или образующегося в результате реакции окрашенного вещества. Измеряя све-топоглощение в соответствующем участке спектра, можно контролировать концентрацию этого вещества. Светопогло-щение пропорционально концентрации окрашенного вещества, измеряется же оно быстро и достаточно точно. [41]
Тем не менее число индикаторных реакций, используемых для определения платиновых металлов кинетическими методами, ограниченно, а для определения платины и родия предложено только по одной методике. [42]
Рассмотрены основные принципы подбора индикаторных реакций для определения микроколичеств элементов кинетическим методом. Показано, что для целенаправленного поиска новых чувствительных и селективных кинетических методов необходимо проводить изучение кинетики и механизма индикаторных реакций. Большое внимание уделено подбору активаторов как одному из важных способов повышения чувствительности кинетических методов анализа. На конкретных примерах рассмотрены возможности повышения селективности кинетических методов анализа. [43]
К способу измерения скорости индикаторной реакции предъявляются требования простоты, надежности и возможности автоматизации. Чувствительность измерения концентрации индикаторных веществ непосредственно связана с пределом обнаружения примеси. В зависимости от природы реакции и индикаторных веществ целесообразно применять соответствующий физико-химический метод измерения скорости реакции. [44]
Из рассмотрения двух уравнений индикаторной реакции для дифениламина можно заключить, что дифенилбензидин должен обладать аналогичным поведением и вызывать меньший расход окислителя в реакции. К сожалению, низкая растворимость дифе-нилбензидина в воде и серной кислоте препятствует его широкому применению. Можно ожидать, что сульфопроизводные дифенил-бензидина будут более подходящими индикаторами. [45]
Страницы: 1 2 3 4