Отдельная реакция
Cтраница 2
Отдельными реакциями будем считать реакции, в которых обычные методы не позволяют выявить промежуточные продукты. При таком условном определении элементарные реакции нельзя отличить от реакций, которые протекают через образование нестабильных форм. [16]
Каждая отдельная реакция тоже должна быть продумана, спланирована заранее. Существует большое число препаративных методов, решающих в принципе одни и те же задачи. Необходимо выбрать тот метод, который позволит достичь наилучшего результата. [17]
Рассмотрим отдельные реакции галогенопроизводных. [18]
Рассмотрим отдельные реакции замещения, обращая внимание на природу атакующего агента. [19]
Рассмотрим отдельные реакции замещения, перечень которых приведен на рис. 22 - 7, обращая внимание на природу замещающего агента и применимость этих реакций для синтеза различных классов ароматических соединений. [20]
Рассмотрим отдельные реакции замещения, обращая внимание на природу атакующего агента. [21]
Рассмотрим отдельные реакции замещения, перечень которых приведен на рис. 22 - 7, обращая внимание на природу замещающего агента и применимость этих реакций для синтеза различных классов ароматических соединений. [22]
Известны отдельные реакции окисления Мп2 1 до МпО с применением таких окислителей, как двуокиси свинца РЬОа в концентрированной азотной кислоте, висмутата натрия НаВЮ3 и персульфата аммония ( NH4) 2S2O8 в слабокислой среде. [23]
Известны отдельные реакции окисления Мп2 до Мп04 с применением таких окислителей, как двуокиси свинца РЬО2 в концентрированной азотной кислоте, висмутата натрия NaBiO3 и персульфата аммония ( NH4) 2Sj O8 в слабокислой среде. [24]
Рассмотрим теперь отдельные реакции схемы и те выводы, которые можно было сделать на основании этих реакций. [25]
Известны отдельные реакции окисления Мп 2до МпО Г1 с применением таких окислителей, как двуокиси свинца - РЬОз в концентрированной азотной кислоте, висмутата натрия NaBiOs и лерсульфата аммония ( NH4hS2O8 в слабокислой среде. [26]
Скорость отдельных реакций и, соответственно, скорость образования побочных продуктов зависит от условий проведения процесса. На скорость суммарной реакции, селективность процесса и выход ацетальдегида существенно влияет состав катали-заторного раствора ( содержание PdCl2, СиС12 и FeCl2), кислотность среды, давление, температура, соотношение этилена и окисляющего агента. [27]
Роль отдельных реакций в механизме действия обратимых систем наглядно иллюстрируется на примере системы, состоящей из гидроперекиси нзопропилбензо. [28]
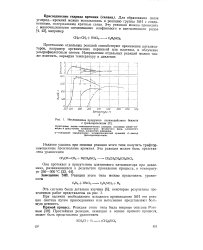 |
Исследование продуктов взаимодействия бензола с трихлорсиланом. [29] |
Протеканию отдельных реакций способствуют применение катализаторов, например органических перекисей или платины, и облучение ультрафиолетовым светом. [30]
Страницы: 1 2 3 4