Анодная катодная реакция
Cтраница 1
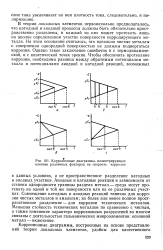 |
Коррозионные диаграммы, иллюстрирующие влияние различных факторов на скорость коррозии. [1] |
Анодные и катодные реакции в зависимости от степени однородности границы раздела металл - среда могут протекать на одной и той же поверхности или на ее различных участках. Совмещение катодных и анодных реакций типично для коррозии чистых металлов и амальгам; их более или менее полное пространственное разделение - для коррозии технических металлов. Меньшая стойкость технических металлов по сравнению с чистым, а также изменение характера коррозионных разрушений во многом связаны с деятельностью гальванических микроэлементов: основной металл - включение. [2]
Анодные и катодные реакции с количественной стороны были изучены еще в 30 - х гг. XIX в. Им были установлены следующие два закона электролиза. [3]
 |
Кривая плотность тока - по-тенциал для растворения металла. [4] |
Анодные и катодные реакции могут протекать на поверхности металла в пространственно разделенных точках. [5]
Анодные и катодные реакции при коррозии стали в пластовых водах могут активизироваться или тормозиться в зависимости от присутствия ионов некоторых солей. [6]
 |
Схема коррозии стали в растворе H2SO4 с выделением водорода. [7] |
Кроме анодных и катодных реакций при электрохимической коррозии происходит движение электронов в металле и ионов в электролите. [8]
Протекание анодной и катодной реакции при электрохимическом процессе коррозии в сущности аналогично процессу, происходящему в гальваническом элементе. [9]
Кроме анодных и катодных реакций при электрохимической коррозии происходит движение электронов в металле и ионов в электролите. Электролитами могут быть растворы солей, кислот и оснований, морская вода, почвенная вода, вода атмосферы, содержащая СО2, SO2, О2 и другие газы. [10]
 |
Внешний вид батареи гидразин-перекисьводородных ТЭ фирмы Альстом мощностью 1 6 - 2 кВт [ Л. 95 ]. [11] |
В результате анодных и катодных реакций концентрация основания в католите повышается, а в анолите понижается. [12]
Разделение коррозионного процесса на самостоятельные анодные и катодные реакции обусловливается существованием ионов металла в растворе и свободных электронов в металле. Из рис. 3 видно, что внутренняя связь анода и катода осуществляется металлом, а внешняя - жидким электролитом, контактирующим с анодными и катодными участками на металлической поверхности. [13]
Для обеспечения высоких скоростей анодных и катодных реакций необходимо применять катализаторы. Активными катализаторами анодного окисления водорода являются платиновые металлы и их сплавы, например Pt-Pd. [14]
В основу понятия об анодных и катодных реакциях положено только представление об определенном направлении тока, но не о величине электродного потенциала. В аккумуляторе, например, положительный электрод при разрядке является катодом, а отрицательный - анодом; при зарядке - наоборот. [15]
Страницы: 1 2 3 4