Анодная катодная реакция
Cтраница 2
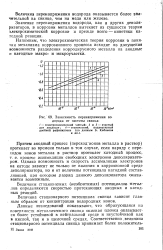 |
Зависимость перенапряжения водорода от чистоты свинца. [16] |
Величины стационарных ( необратимых) потенциалов металлов определяются скоростью протекающих анодных и катодных реакций. [17]
 |
Сопряжение процессов катодного восстановления металла ( 1, 2 ц анодного окисления восстановителя ( 3 4 на поверхности металла. [18] |
Электрохимические исследования вместе с тем показали [50], что сопряжение анодных и катодных реакций во многих случаях осуществляется более сложным образом, чем это описано выше, - наблюдается взаимное влияние электрохимических реакций. [19]
При протекании коррозионного тока в системе происходит смещение значений электродного потенциала анодной и катодной реакции в направлении их сближения. Обычно анодная и катодная кривые не пересекаются ( поверхность металла не становится эквипотенциальной), за счет определенного омического сопротивления электролита. Значение стационарного потенциала V cm металла или сплава ( соответствующее пересечению кри-аых) в общем случае определяется ( см. рис. 10) соотношением скоростей анодной и катодной реакции при максимальном токе коррозии / max. Степень наклона поляризационных кривых характеризует большую ( крутой ход) или малую ( пологий ход) затрудненность протекания электродных реакций. [20]
При воздействии блуждающих токов на подземные металлические трубопроводы процесс электролиза сопровождается анодными и катодными реакциями, протекающими на границе металл - грунт. Основной анодной реакцией является растворение стали. Основными катодными реакциями являются ионизация кислорода или выделение водорода. [21]
Здесь аа и ак - кажущиеся, или эффективные, коэффициенты переноса анодной и катодной реакции. Их связь с истинными коэффициентами переноса а и ак ( а ак 1; аа 0; ак 0) определяется механизмом реакций. [22]
 |
Схематическое изображение анодных кривых для основной части зерна ( / и границ зерен ( / / ( 8 ] однофазной нержавеющей стали. [23] |
Поскольку величина стационарного потенциала для двух-электродной системы определяется пересечением суммарных поляризационных кривых для анодной и катодной реакции, можно соответствующим подбором концентраций активаторов и окислителей ( деполяризаторов) сместить стационарный потенциал до таких значений, при которых будет наблюдаться преимущественное растворение границ зерен. Условия, обеспечивающие выявление межкристаллитной коррозии, авторы определяют из диаграммы, представленной на рис. 143, где схематически изображена суммарная анодная кривая / для стали, склонной к межкристаллитной коррозии, и анодная кривая / / для зерен, аналогичная анодной кривой для стали, не склонной к межкристаллитной коррозии. [24]
Значения р ( соответствующие w), при которых обеспечено минимальное суммарное торможение анодной и катодной реакции, являются наиболее опасными в отношении коррозии. [25]
 |
Электрическая схема замкнутой коррозионной пары. [26] |
Устойчивое во времени значение неравновесного ( необратимого) электродного потенциала металла, соответствующее равенству сумм скоростей анодных и катодных реакций, называют стационарным потенциалом металла. [27]
 |
Схема прибора для электрохимических исследований щелевой коррозии. А - анолит. К - католит. [28] |
Прежде всего в узкий зазор резко затрудняется доступ кислорода, и это обусловливает ряд особенностей протекания анодных и катодных реакций. Представленные на рис. 86 поляризационные кривые для железа, находящегося в зазорах, показывают, что в нейтральных электролитах скорость анодного процесса в зазоре заметно увеличивается, а катодного - тормозится. [29]
К электрохимическим методам борьбы с коррозией относятся такие, в основе которых лежит принцип непосредственного воздействия на скорость протекания сопряженных анодных и катодных реакций. Прежде всего это выражается в изменении потенциала защищаемого металла. Различают катодную и анодную электрохимическую защиту. [30]
Страницы: 1 2 3 4