Очень быстрая реакция
Cтраница 3
С развитием методов изучения очень быстрых реакций ( см. обзоры [14, 16, 17]) удалось показать, что величины Дц0 для переноса протона от атомов кислорода или азота одной молекулы к атомам азота или кислорода другой молекулы равны нулю или отрицательны, а удельные скорости, за некоторыми исключениями, равны скоростям диффузии участвующих молекул. Исключения представляют те случаи, когда переносимый протон связан в реагенте внутримолекулярной водородной связью. Но когда Ац0 положительно и в одном направлении процесс лимитируется диффузией, то удельная скорость обратного процесса меньше, чем скорость диффузии. [31]
А В пределе при очень быстрой реакции ( н с - -) кр - Когда глубина ее проникновения сравнима с диаметром пор, работает только внешняя поверхность частицы, и скорость реакции пропорциональна внешней поверхности гранул катализатора. [32]
Лишь для небольшого числа очень быстрых реакций перенос реагирующих веществ к внешней поверхности зерен контакта определяет суммарную скорость процесса. В этих случаях разность температур поверхности контакта и газового потока на начальных стадиях приближается к величине теоретического разогрева. Для реакций, тормозящихся продуктом, перенос к внешней поверхности сказывается лишь на первых стадиях и не влияет существенно на общую интенсивность процесса. Однако разность температур поверхности контакта и газового потока достигает для этих реакций на первых стадиях заметной величины, что сказывается на важном технологическом параметре - минимально допустимой температуре входа газа в контактную массу. При высоких давлениях промышленные каталитические реакции осуществляются при значениях критерия Рейнольдса порядка тысяч и даже десятков тысяч, и, соответственно этому, процессы переноса к внешней поверхности протекают с большой скоростью. Для рассмотренных процессов ( синтез аммиака, метанола, ряд реакций гидрирования) не обнаружено заметного влияния процессов переноса к внешней поверхности зерен контакта на суммарную скорость. [33]
Недавно для измерения скоростей очень быстрых реакций применили ударную трубу. В таком устройстве удается достигнуть времени пребывания от 20 мсек до долей миллисекунды и можно определить константы скорости реакций в пределах 0 1 - 200 сек 1 и даже выше. [34]
Случай 1 относится к очень быстрым реакциям. Таким образом, в случае быстрых реакций ( согласно этому уравнению) доля непревращенного реагента определяется только механизмом движения ожижающего агента ( поскольку X полностью зависит от свойств пузырей), но не природой самой реакции. [35]
Тем не менее при очень быстрых реакциях могут наблюдаться температурные градиенты. [37]
После 1947 года для изучения очень быстрых реакций был разработан целый ряд приборов, и представляется более важным скорее их использовать, нежели продолжать дальнейшее усовершенствование и создание более сложного оборудования. Проблемы, техники и применения нового оборудования к хорошо известным электродным процессам должны были бы привлекать меньше внимания, нежели более фундаментальные задачи. [38]
Имеется ценная информация о кинетике очень быстрых реакций, идущих с разрывом О - Н - связи, важная для суждения о водородном обмене. [39]
 |
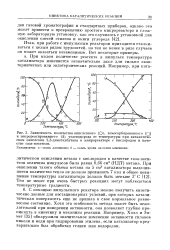
График функции С ( т. [40] |
Большой может быть сегрегация в случае очень быстрых реакций: за время их протекания частицы не успевают перемешаться. [41]
Методы изотопного обмена также, позволяют изучать очень быстрые реакции, хотя следует отметить, что этот метод можно применять лишь к таким реакциям, механизм которых связан с обменными процессами. Сама по себе реакция может протекать исключительно быстро, однако оказывается возможным измерить ее скорость, так как перераспределение нуклидов в ходе реакции происходит за счет многократного обмена в прямом и обратном направлениях, и поэтому оно происходит значительно медленнее, чем происходит сама реакция обмена. Для изучения очень быстрых химических реакций, а также для установления короткоживущих промежуточных продуктов применяется метод парамагнитного электронного резонанса. К наиболее быстрым химическим реакциям, для которых константа скорости практически идентична числу столкновений ( ktt 1012 с -), относятся реакции переноса протона, а также различные реакции с электронными переходами. Совсем недавно для определения констант скорости с большим успехом применяют релаксационные методы. Скорость установления нового равновесного состояния регистрируется, например, на осциллографе. Время, необходимое для перехода к новому состоянию, называют временем релаксации; оно количественно связано с константой скорости реакции. Для нарушения равновесия используют также кратковременное повышение температуры. [42]
Некоторые типы абсорбционных колонн могут применяться для очень быстрых реакций, особенно когда должен быть переработан довольно большой поток газа. [43]
Предлагаемый метод не должен предусматривать измерения скоростей очень быстрых реакций. [44]
Со смешением приходится в основном встречаться в случае очень быстрых реакций как в гомогенных, так и в гетерогенных системах. [45]
Страницы: 1 2 3 4