Нуклеофильная реакция
Cтраница 3
Значения а для нуклеофильных реакций обычно близки к соответствующим значениям, найденным для реакций второго порядка общего основного катализа. Бендер и Тернквист [83], однако, указали, что в этом случае верхний предел значений а отличен от единицы. Это связано с упомянутым выше занижением параметра а для гидроксильного иона, наблюдаемым и для нуклеофильных реакций ( см. график для оксианионов, стр. Однако приведенная этими авторами величина а1 62 не может служить подтверждением изложенных ими соображений, поскольку она рассчитана ретроспективно из графика, использующего данные, относящиеся к основаниям различных классов. [31]
Одной из наиболее часто применяемых нуклеофильных реакций нитрильной группы является реакция Риттера, которая проводится в присутствии серной кислоты и других протонных кислот и приводит к образованию новой связи N-С. Большое теоретическое и практическое значение имеют реакции нитрилов в присутствии апротонных кислот, в результате которых образуются нитри-лиевые соли и продукты их превращения. В данной главе рассмотрены также реакции нитрилов с хлорангидридами карбоновых кислот, которые осуществляются в присутствии апротонных кислот или без применения каких-либо катализаторов, нуклеофильные реакции нитрилов с различными трехчленными циклами, завершающиеся расширением циклов или получением соединений линейного строения, оригинальные стереоспецифические реакции одновременного воздействия на олефины нитрилов ( играющих в данном случае роль нуклеофильных соединений) и некоторых элек-трофильных реагентов. Завершается глава описанием ряда малоизвестных или недостаточно исследованных реакций нитрилов, приводящих к образованию новой связи N-С. [32]
По отношению к нуклеофильным реакциям наиболее реак-ционноспособны атомы с минимальной нуклеофильной энергией локализации, наибольшим индексом свободной валентности и наименьшей электронной плотностью. [33]
Большой интерес к нуклеофильным реакциям нитрилов, главными продуктами которых являются N-замещенные амиды, обусловливает поиски новых путей осуществления этих реакций. В последние 15 лет опубликованы данные о проведении нуклео-фильных реакций нитрилов с образованием новых связей N-С под действием кислых реагентов, ранее для этой цели не использовавшихся, щелочных реагентов и электрохимическим путем. [34]
По аналогии с нуклеофильными реакциями легко протекающая электрофильная реакция, сопровождаемая второй ( каталитической) реакцией под влиянием функциональной группы в исходном электрофиле, и, наконец, распадом на конечные продукты с регенерацией электрофила, должна также приводить к каталитическому действию. [35]
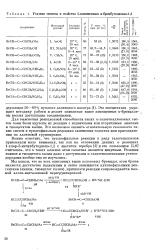 |
Условия синтеза и свойства 4-замещенных - бромбутадиенов-1 2. [36] |
Важно отметить, что нуклеофильные реакции в ряду галогеналленоа привлекали мало внимания, так как на основании данных о реакциях 1-хлор - 3-метшгбутадиена - 1 2 с ацетатом серебра [4] и его сольволиза [5,6] считалось, что в таких алленах атом галогена является инертным. Реакций-аминов и тиоацетата калия даже с доступными а-галогеналленовыми углеводородами вообще еще не изучались. [37]
И электрофильные, и нуклеофильные реакции называются гетеро-литическими реакциями. [38]
Можно думать, что нуклеофильные реакции обмена возможны с участием соединений, содержащих отрицательно заряженный водород, например с участием гидридов металлов [527], однако такие процессы совершенно не исследованы в области органической химии ( см. дополнение 9 на стр. [39]
В табл. 3 приведены наиболее важные нуклеофильные реакции альдегидов и кетонов. [40]
В некоторых случаях наблюдается внутримолекулярная нуклеофильная реакция нитрильной группы с положительно заряженным атомом фосфора в фосфазе-нах. [41]
 |
Характеристические константы скорости замещения Н2О во внутренней координационной сфере ионов металлов ( абсцисса в с -. Из работы. Eigen M., Pure Appl Chem, 6, 105 ( 1963. [42] |
Он характерен для многих нуклеофильных реакций органических соединений. [43]
Кроме того, в ходе нуклеофильных реакций в ряду циклогексана часто получаются не столько продукты замещения, сколько продукты реакций отщепления и перегруппировок; эти продукты образуются преимущественно при реакциях экваториальных заместителей. [44]
Кинетическое исследование некоторых из этих нуклеофильных реакций показало, что аминолиз и алкоголиз протекают по бимолекулярному механизму присоединения-отщепления, как и нейтральный гидролиз имидазолидов арилкарбоновых кислот. [45]
Страницы: 1 2 3 4