Плазмохимическая реакция
Cтраница 1
Плазмохимические реакции, для к-рых с повышением т-ры увеличивается равновесная концентрация промежут. При этом скорости р-ций очень велики ( длительность контакта реагентов может составлять 10 - 3 - 10 - 3 с), что позволяет создавать миниатюрную аппаратуру. Кроме того, используют р-ции в неравновесной плазме. [1]
Плазмохимические реакции, протекающие в неравновесных условиях, проводят в тлеющем и импульсном разрядах, в ВЧ-тлеющем разряде, СВЧ-плазмотронах, под действием концентрированного излучения оптических квантовых генераторов, а также в плазме, образованной ударными волнами или быстрым адиабатическим сжатием. [2]
Плазмохимические реакции Протекают, как правило, в неравновесных условиях. Кинетика таких процессов отличается от обычной химической кинетики. Неравновесная химическая кинетика учитывает квантовую энергетическую структуру атомно-молеку-лярных частиц, переходы между различными энергетическими состояниями и вероятность протекания различных химических реакций. [3]
Плазмохимические реакции могут быть неравновесными и ( квази) - равновесными. В табл. 1 показаны типы плазмохимических реакций. [4]
Условно плазмохимические реакции можно разделить на неравновесные и квазиравновесные. Примером первых являются реакции в газоразрядной плазме низкого давления. Они характеризуются сильным отклонением системы от равновесия. При малом давлении эффективность передачи энергии от электронов к тяжелым частицам низка, но так как энергию от внешнего электрического поля получают практически только самые легкие заряженные частицы - электроны, их средняя энергия оказывается намного выше средней энергии тяжелых частиц. Эффективная температура электронного газа достигает десятков тысяч градусов, в то время как температура газа тяжелых частиц может быть близка к комнатной. Следствием отрыва электронной температуры от температуры газа тяжелых частиц является определяющая роль электронных соударений в образовании химически активных частиц и последующем протекании химических реакций. [5]
Константы скоростей плазмохимических реакций, протекающих при температурах выше 2500 К, определяются в ударных трубах или методом адиабатического сжатия. [6]
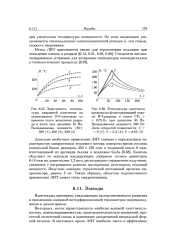
В случае проведения плазмохимических реакций с использованием в качестве реагентов конденсированных веществ наблюдается сильное взаимное влияние факторов, связанных с протеканием химических процессов и процессов тепло-и массообмена. В работе [92] предложена математическая модель, описывающая поведение частиц, введенных в плазменную струю; при этом были сделаны следующие основные допущения: порошок по сечению канала анодного сопла распределен равномерно, температура и скорость газа по сечению канала распределены равномерно, частицы порошка имеют сферическую форму, температура по сечению частиц постоянна. Для получения более общих представлений о поведении конденсированных частиц в плазменной струе были рассмотрены некоторые системы газ - материал, которые представляют крайние случаи сочетания теплофизических свойств: аргон-вольфрам, водород-трехокись вольфрама. [7]
Перечисленные пять особенностей плазмохимических реакций представляют собой, говоря по существу, характерные черты неравновесных химических процессов, частным ( хотя и очень важным) случаем которых являются реакции в низкотемпературной плазме. В настоящем пункте излагаются некоторые специфические черты именно плазмохимических реакций. [8]
Другой специфической проблемой кинетики плазмохимических реакций, на которой мы здесь остановимся, является определение размеров реактора для процессов в плазменной струе. [9]
Анализ специфического неравновесного характера плазмохимических реакций позволяет не только понять закономерности этих реакций, но и обосновать зыбор путей их практической реализации. [10]
Одной из специфических проблем кинетики плазмохимических реакций является создание условий, обеспечивающих быстрое охлаждение плазменной струи во время протекания реакции в определенных пространственно-временных интервалах. Если скорость охлаждения будет недостаточно велика, то целевые продукты реакции успеют разложиться и эффективность процесса окажется малой. Следует рассмотреть два типа закалки: принудительную закалку и автозакалку. [11]
По мере нагревания увеличивается тепловыделение плазмохимической реакции и, тем самым, скорость нагревания. [13]
Таким образом, при проведении плазмохимических реакций выдерживают следующие параметры: Г 2000 - 20 000 К, Р 1 Па - 5 МПа. Обычно это низкотемпературная плазма. [14]
Поскольку единой общей теории кинетики плазмохимических реакций ( как части неравновесной химической кинетики) еще не существует, большое значение приобретает изучение особенностей простейших, часто встречающихся ( и в какой-то мере модельных) реакций. [15]
Страницы: 1 2 3 4