Последующая химическая реакция
Cтраница 2
В щелочных средах процесс осложняется последующими химическими реакциями. [16]
Продукты крекинг-процесса могут быть превращены последующими химическими реакциями во множество других ценных химических продуктов. [17]
 |
Хронопотен-циометрическая кривая для двухступенчатой. [18] |
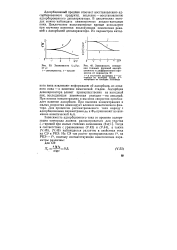
Если после обратимой электрохимической стадии протекает последующая химическая реакция, то при увеличении константы скорости этой реакции происходит сдвиг кривой к более низким значениям потенциала. [19]
При выводе зависимостей было принято, что последующая химическая реакция протекает с большой скоростью. [20]
В связи с потреблением продукта восстановления в последующей химической реакции наблюдается относительно меньшее возрастание анодного пика со скоростью v, чем в отсутствие химической реакции. [21]
Приведенные уравнения для обратимого электродного процесса с последующей химической реакцией первого порядка, в которую вступает первичный продукт электродной реакции, имеют сходную форму. [22]
Адсорбция деполяризатора влияет преимущественно на катодный пик, последующая химическая реакция - на анодный. При низких концентрациях и высоких скоростях преобладает влияние адсорбции. При высоких концентрациях и малых скоростях доминирует влияние кинетического фактора. [24]
Лимитирующими стадиями электродного процесса могут быть предшествующие или последующие химические реакции. [25]
Из уравнения (18.7) следует, что в случае необратимой последующей химической реакции переходное время процесса окисления не зависит от времени восстановления ( за исключением коротких времен восстановления), однако меняется с изменением плотности применяемого тока. [26]
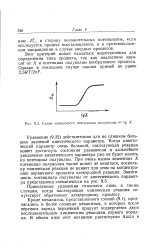 |
Схема зависимости потенциала полуволны от lg X. [27] |
Приведенные уравнения относятся лишь к таким случаям, когда последующая химическая реакция сопутствует обратимому электродному процессу. [28]
При этом предельный каталитический ток, как и при последующей химической реакции, не может превысить предельный диффузионный ток субстрата, который для ионов металлов часто можно наблюдать в виде отдельной волны, находящейся при более отрицательных потенциалах. [29]
Иногда образование радикала ( при электровосстановлении га-лоидпроизводных) является результатом последующей химической реакции, в которую вступает образовавшийся при переносе электрона анион-радикал. [30]
Страницы: 1 2 3 4