Быстрая химическая реакция
Cтраница 1
Быстрые химические реакции могут протекать между полупроводником и соединениями донора или акцептора. [1]
Для быстрых химических реакций реакционная зона может иметь принципиально неопределенную, но реально - конечную протяженность. Тогда необходимость замыкания потока отпадает. Другие варианты организации работы аппарата при Р О или W О вытекают непосредственно из анализа статики НСРРП, как обеспечивающие наивысшие конверсии реагентов. [2]
При быстрой химической реакции в высокотемпературной смеси молекулы, обладающие большой энергией, могут быстрее превратиться в конечные продукты, чем в результате соударений пополнится их количество. [3]
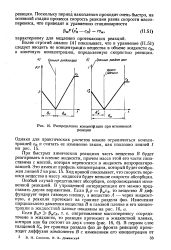 |
Распределение концентрации при мгновенной реакции. [4] |
При быстрых химических реакциях часть вещества В будет реагировать в пленке жидкости, причем масса этой его части сопоставима с массой, которая переносится в жидкость непрореагировавшей. Ход кривой показывает, что скорость переноса вещества в массу жидкости будет меньше скорости абсорбции. [5]
При весьма быстрых химических реакциях наиболее медленными стадиями гетерогенного каталитического процесса оказываются диффузионные процессы подвода и отвода вещества к внешней и внутренней поверхностям катализатора. Реакция, как говорят, протекает во внешней или внутренней диффузионных областях. [6]
 |
Блок-схема установки для регистрации изменения пропускания в заданной точке спектра. [7] |
При изучении быстрых химических реакций основные трудности связаны с регистрацией изменения излучения и инициированием реакций. Регистрация изменения во времени спектрального излучения может осуществляться двумя путями: регистрацией изменения излучения в одной длине волны ( или нескольких длинах волн) и быстрым измерением спектра ( или серии спектров) с помощью скоростного спектрометра. [8]
При наличии быстрой химической реакции между А и В уменьшается расстояние, которое газ должен пройти в жидкости. Необходимость в дальнейшей диффузии газа отпадает и скорость процесса увеличивается. [9]
При наличии быстрой химической реакции между А к В уменьшается расстояние, которое газ должен пройти в жидкости. Необходимость в дальнейшей диффузии газа отпадает и скорость процесса увеличивается. [10]
В пламени протекает быстрая химическая реакция в узком интервале температуры, примыкающем к температуре горения. [11]
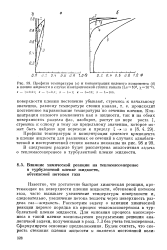 |
Профили температуры ( а и концентрации целевого компонента ( б в пленке жидкости в случае изотермической стенки канала ( Le103, хЮ 2. 1 - - 2 - . 3 - . 1. 4 - . 10. я - . 100. [12] |
Известно, что достаточно быстрая химическая реакция, протекающая на поверхности пленки жидкости, обтекаемой потоком газа, часто вызывает увеличение температуры поверхности и, следовательно, увеличение потока теплоты через поверхность раздела газ-жидкость. Рассмотрим задачу о влиянии химической реакции первого порядка на процесс тепломассопереноса в турбулентной пленке жидкости. Для описания процесса массопере-носа в такой пленке воспользуемся результатами решения аналогичной задачи, полученными в разд. [13]
Для массопередачи с быстрой химической реакцией значительное снижение скорости реакции и увеличение интенсивности перемешивания приводит к переходу из режима массопередачи с быстрой реакцией к массопередаче в смешанном режиме или в кинетическом режиме с реакцией в объеме фаз. В последнем случае скорость процесса уже не зависит от поверхности раздела фаз. Подобное изменение вызвано тем, что при достаточном уменьшении скоро сти реакции) ю пути диффузии равновесие не дости гается, а увеличение скорости массопередачи приводит к реакции в объеме принимающей фазы. [14]
Оптимальные условия для протекания быстрых химических реакций создаются в случае выполнения отношения характерных времен химической реакции и смешения тсмтх. Изменяя геометрию ( дизайн) зоны реакции, динамику, а также физические параметры жидких потоков, можно оптимизировать значения характеристик турбулентного смешения в соответствии со спецификой процесса, тем самым воздействуя на характер его протекания. [15]
Страницы: 1 2 3 4 5