Быстрая химическая реакция
Cтраница 3
В одном, предельном, случае протекает настолько быстрая химическая реакция, что скорость диффузии веществ целиком лимитирует общую скорость процесса. В другом случае химическая реакция протекает настолько медленно, что газообразный реагент абсорбируется жидкостью и достаточно равномерно распределяется в ней, при этом общая скорость процесса целиком определяется скоростью химической реакции. [31]
Реакция обмена галоген-литий - одна из самых быстрых химических реакций, и проведение ее при низких температурах позволяет не затрагивать присутствующие в соединении функциональные группы, которые легко реагируют с карбанионами. [32]
Наряду с применением этого метода к изучению быстрых химических реакций, о чем кратко упоминалось выше, этот метод очень удобен для исследования почти обратимых систем в более широкой области потенциалов. Он является также весьма чувствительным методом для изучения адсорбции как неорганических, так и органических деполяризаторов. [33]
Основные научные исследования посвящены кинетике и механизму быстрых химических реакций Создал уникальные установки большой мощности для импульсного фотолиза. [34]
Другим предельным случаем является медленная адсорбция вещества и быстрая химическая реакция на поверхности. Такой процесс называется химической адсорбцией или хемосорбцией. Здесь адсорбированные молекулы связываются с поверхностью химическими силами того же типа, что и силы, осуществляющие валентную связь. Для того чтобы эти силы действовали, молекула должна перейти в деформированное состояние и преодолеть активационный барьер. Поэтому химическая адсорбция требует энергии активации. Иногда ее называют активированной адсорбцией. Химическая адсорбция тесно связана с процессом гетерогенного катализа. [35]
Возможен и другой механизм распространения в пространстве зоны быстрой химической реакции, при котором каждый последующий слой газа нагревается не теплопроводностью, а путем быстрого сжатия, достаточно интенсивного, чтобы довести реагирующую среду до состояния адиабатического воспламенения. Такой механизм горения, именуемый детонацией, в принципе отличающийся от дефлаграционного, характеризуется рядом особенностей, порождающих сложные задачи для техники взрывобезопасности. Для понимания закономерностей детонационного горения необходимо установить, в каких условиях происходит нагревание сжатием до столь высоких температур. [36]
Влияние дополнительного времени сильнее всего проявляется при проведении быстрых химических реакций. В этом случае явно невыгодно использовать реакторы периодического действия. И наоборот, для реакций, протекающих медленно и в малом объеме, могут применяться реакторы периодического действия. [37]
В этом процессе вслед за первоначальным переносом электрона осуществляется быстрая химическая реакция, продукт которой претерпевает дальнейшее окисление при том же или более низком потенциале. [38]
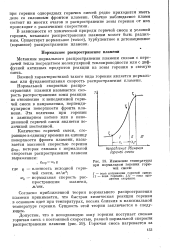 |
Изменение температуры при нормальном горении горючей смеси. [39] |
Согласно приближенной теории нормального распространения пламени принимается, что быстрая химическая реакция горения в основном идет при температурах, весьма близких к максимальной температуре горения. Сущность этой теории заключается в следующем. [40]
Деполяризациейпая схема, в которой деполяризатор образуется в результате быстрой химической реакции из электронеактивного вещества, катализируемой побочным продуктом электродного процесса, встречается при электролизе формальдегида в недостаточно забуференных растворах. Решение задачи [12] дает возможность вычислить абсолютные величины предельных токов при помощи кинетических констант реакции образования деполяризатора, которые были получены из предельных токов формальдегида в буферной среде. Экспериментальные результаты Брдички [16] полиостью соответствуют выводам теории. [41]
Перечислим кратко основные экспериментальные методы получения информации о механизмах быстрых химических реакций и их кинетике: 1) струевые методы; 2) спектроскопические методы; 3 релаксационные методы; 4) метод молекулярных пучков; 5) импульсный фотолиз и радиолиз; 6) зондовые методы; 7) резонансная хемилюминесценция. [42]
При помощи масс-спектрометра с быстрой разверткой удобно исследовать кинетику быстрых химических реакции, в которых участвуют промежуточные продукты и свободные радикалы при низких концентрациях. Кроме высокой аналитической точности прибора, желательно иметь максимальную чувствительность, удобную систему напуска и развертку в широком диапазоне масс. Для обеспечения этих требований разработан масс-спектрометр с циклоидальной фокусировкой, сочетающий совершенную фокусировку и высокую эффективность собирания ионов с быстрой регистрацией, осуществляемой электронным умножителем. [43]
Вторая волна восстановления соответствует необратимому переносу электрона с параллельно-протекающей быстрой химической реакцией ( димеризацией кетильных радикалов), и ее форма подчиняется соответствующему уравнению Майрановского [3], особенно в средах с высоким содержанием спирта, где снижается искажающий картину эффект торможения адсорбированными на электроде димерами. [44]
Вторая волна восстановления соответствует необратимому переносу электрона с параллельнотфотекающей быстрой химической реакцией ( димеризацией кетильных радикалов), и ее форма подчиняется соответствующему уравнению Майрановского [3], особенно в средах с высоким содержанием спирта, где снижается искажающий картину эффект торможения адсорбированными на электроде димерами. [45]
Страницы: 1 2 3 4 5