Значение - атомный радиус
Cтраница 1
Значения атомных радиусов ( в 10 - м или 10 - 8 см) получены путем деления на два межатомных расстояния в кристаллических структурах простых тел с координационным числом КЧ-12. [1]
Значения атомных радиусов и объемов циркония и гафния, а также ионных радиусов Zr4 и Hf4 очень близки. [2]
Значения атомных радиусов европия и иттербия ложатся почти на прямую линию, проведенную от бария к свинцу. [3]
Каковы значения эффективных атомных радиусов неона, аргона, криптона и ксенона, вычисленные на основаии информации, содержащейся - в предшествующем примере. [4]
Как изменяются значения атомных радиусов в периодах и подгруппах. [5]
Практически совпадают значения атомных радиусов для молибдена и вольфрама, хотя эти элементы являются представителями разных периодов Системы. Обусловлено это тем, что увеличение радиусов в результате возрастания числа электронных слоев при переходе от V к VI периоду компенсируется 4 / - сжатием при заполнении / - орбитали у лантаноидов. Поскольку лантаноиды вклиниваются в самом начале d - элементов VI периода, последующие за лими элементы вставной декады характеризуются аномально низкими величинами эффективных атомных радиусов. [6]
Скандий по значению атомного радиуса и энтальпии образования оксида ближе стоит к А1, чем к своим более тяжелым электронным аналогам. Гидроксид скандия - слабое основание с ак-фотерными свойствами; соли Sc4 подвергаются заметному гидролизу. Между солями скандия и лантаноидами не всегда наблюдается изоморфизм. Скандий в большей степени, чем его электронные аналоги, склонен давать комплексные соединения. [7]
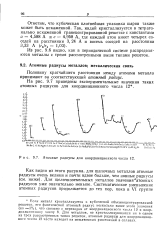 |
Атомные радиусы для координационного числа 12. [8] |
Для щелочноземельных металлов значения атомных радиусов уже значительно меньше. [9]
У переходных металлов значения атомных радиусов возрастают в пределах группы с увеличением атомного номера, уменьшаются в периоде от побочной подгруппы III группы до VIII группы и затем снова возрастают от VIII группы до побочной подгруппы II группы. [10]
Для инертных газов даны значения атомных радиусов. [11]
В табл. 1 даны значения атомного радиуса, потенциалов, возбуждения, наименьших потенциалов ионизации и работы выхода для некоторых наиболее часто встречающихся при сварке элементов периодической системы, а также энергия сродства к электрону. [12]
Для инертных газов даны значения атомных радиусов. [13]
 |
Радиус эффективного действия молекулы хлора. [14] |
В табл. 3 приведены некоторые значения атомных радиусов и углов. [15]
Страницы: 1 2 3 4