Редокс-потенциал
Cтраница 3
Вольтамперометрические измерения редокс-потенциалов ( табл. 1.18) ряда изоиндолов показали, что эта система очень чувствительна к восстановлению. [31]
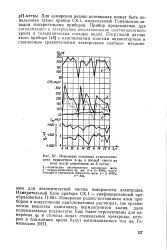 |
Изменение основных технологических параметров и фо в иловой смеси на воде после аэротенков за 3 суток. [32] |
Для измерения редокс-потенциала может быть использован также прибор СХ-1, выпускаемый Гомельским заводом измерительных приборов. [33]
Пользуясь таблицами редокс-потенциалов и зная, что в качестве окислителя всегда действует ОФ системы с большим алгебраическим значением потенциала, можно определить возможность и направленность тех или иных окислительно-восстановительных реакций. При одинаковом или очень близком значении электродных потенциалов двух систем реакция между ними не имеет преимущественного направления и обе системы находятся в состоянии подвижного равновесия. Различие между редокс-потенциалами таких систем можно увеличить повышением концентрации ОФ одной системы и ВФ другой, в результате чего появляется возможность направленного процесса. [34]
 |
Схема работы свинцового кислотного аккумулятора при заряде ( а и разряде ( б. [35] |
В ряду редокс-потенциалов ( табл. 19) отмечают следующие закономерности. [36]
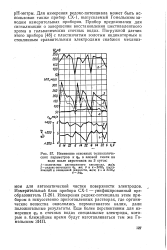 |
Изменение основных технологических параметров и ро в иловой смеси на воде после аэротенков за 3 суток. [37] |
Для измерения редокс-потенциала может быть использован также прибор СХ-1, выпускаемый Гомельским заводом измерительных приборов. Прибор предназначен для сигнализации о завершении восстановления шестивалентного хрома в гальванических сточных водах. [38]
Практическое значение редокс-потенциалов, рассчитанных таким образом, не следует переоценивать, так как полученная величина может не иметь никакой связи с истинным редокс-потен-циалом. [39]
Соотношение между редокс-потенциалом среды и стандартным редокс-потенциалом индикатора определяет соотношение между концентрациями окисленной и восстановленной форм индикатора и, следовательно, окраску раствора. [40]
Таким образом, редокс-потенциал до точки эквивалентности является функцией концентрации циана, а после точки эквивалентности - содержания гипохлорид - ионов. [41]
Каи значение имеют редокс-потенциалы для управления реакциями окисления - восстановления. [42]
Какое значение имеют редокс-потенциалы для управления реакциями окисления - восстановления. [43]
Исходя из значений редокс-потенциалов, наиболее эффективно окислительные процессы должны протекать в слабокислой среде, при рН 5 0, где содержание НСЮ максимально. [44]
Из приведенных значений редокс-потенциалов видно, что окислительные свойства у РЬСЬ выражены сильнее, чем восстановительные. [45]
Страницы: 1 2 3 4