Твердый редоксит
Cтраница 1
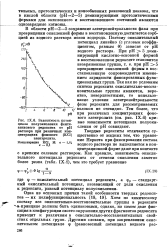 |
Зависимость потенциала полуокисления фенти-азинового редоксита от рН раствора при различных концентрациях фонового ( КС1 электролита. [1] |
Твердые редокситы отличаются существенно от жидких тем, что уравнение Нернста при фиксировании состава водного раствора не выполняется в концентрационной форме даже при контакте с крепким солевым раствором. [2]
У твердых редокситов, функциональные группы которых обладают кислотными или основными свойствами, окислительный потенциал становится функцией активности ионов водорода. Естественно, что время, затрачиваемое для построения зависимости окислительного потенциала от рН, резко возрастает. [3]
В твердом редоксите каждая функциональная группа находит ружении других фрагментов. [4]
Окислительный потенциал твердого редоксита не может быть измерен непосредственно, так как нельзя осуществить прямой обмен электронами между твердым редокситом и индикаторным электродом - Можно воспользоваться свойством твердого редоксита вступать в окислительно-восстановительное взаимодействие с водным раствором обратимой окислительно-восстановительной системы. По достижении равновесия окислительные потенциалы обеих систем станут равными. [5]
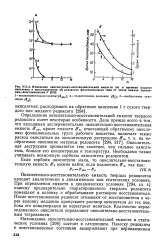 |
Изменение окислительно-восстановительной емкости ( а и времени полного окисления и восстановления ( tf редоксита фентиазинового типа от числа циклов окисления-восстановления N. [6] |
Окислительно-восстановительную емкость твердых редокситов находят аналитически в динамических или статических условиях. [7]
Определение окислительно-восстановительной емкости твердого редоксита имеет некоторые особенности. Окислительная деструкция проявляется тем заметнее, чем сильнее окислитель, больше его концентрация и температура. Необходимо также учитывать возможную сорбцию окислителя редокситом. [8]
Подобно жидким редокситам на твердый редоксит с объемным распределением рабочего вещества накладывается условие электронейтральности. Поэтому окислительный потенциал такого редоксита при малой неионообменной сорбции зависит от активности ионов в водном растворе, поскольку они обеспечивают электронейтральность фаз в системе твердый редоксит - водный раствор. В случае поверхностного распределения рабочего вещества электронейтральность фаз обеспечивается образованием двойного электрического слоя на границе раздела твердый редоксит - водный раствор. Отсюда следует существенное различие в свойствах ре-докситов с разным распределением рабочего вещества. [9]
При рассмотрении гетерогенной системы твердый редоксит - раствор медиатора и реакций, протекающих в ней, во внимание необходимо принимать не только окислительно-восстановительные, но и протолитические процессы. [10]
 |
Схема установки для потенциометрических измерений. [11] |
Кроме того, для твердых редокситов необходима оценка структурных свойств, а для жидких редокситов - коэффициентов распределения компонентов окислительно-восстановительной системы. [12]
Анализ теоретических положений функционирования твердых редокситов, приведенный выше, показал принципиальную возможность использования для оценки окислительно-восстановительных свойств редокс-полимеров экспериментального приема изготовления из них мембран измерительных электродов и определения значений окислительного потенциала последнего в медиаторе. [13]
Точно определить понятие окислительного потенциала твердого редоксита затруднительно [4] ввиду того, что потенциал нерастворимого твердого редоксита не может быть непосредственно измерен на электроде в фазе твердого редоксита, хотя такие попытки и предпринимаются. [14]
Для количественной оценки скорости окислительно-восстановительных превращений твердых редокситов обычно использовались следующие способы: газометрический, химический, электрохимический и метод электронного парамагнитного резонанса. [15]
Страницы: 1 2 3