Кинетический режим
Cтраница 1
 |
Первичный ( П и вторичный ( В слои при растекании жидкости по твердой поверхности [ IS ]. [1] |
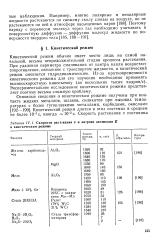
Кинетический режим очень непродолжителен ( 10 - 3 - 10 - 2с) и имеет место лишь на самой начальной стадии процесса. В начале процесса растекания силы молекулярного притяжения, действующие со стороны твердого тела, вытягивают из нижней части капли тонкий слой жидкости - слой Я ( рис. 2.9), толщина которого не превышает радиуса действия межмолекулярных сил. Вслед за этим слоем перемещается более толстый слой В ( несколько мкм) и наконец в движение вовлекается вся масса капли. [2]
 |
Скорости растгкания v и энергии активации Е в кинетическом режиме. [3] |
Кинетический режим обычно имеет место лишь на самой начальной, весьма непродолжительной стадии процесса растекания. При удалении периметра смачивания от центра капли возрастает сопротивление, связанное с транспортом жидкости, и кинетический режим сменяется гидродинамическим. Экспериментальное исследование кинетического режима представляет поэтому весьма сложную проблему. [4]
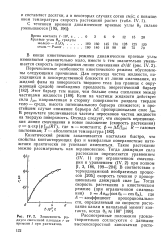 |
Зависимость Ра - Рассмотренные положения удовле. [5] |
Кинетический режим заканчивается настолько быстро, что свойства контактирующих фаз и межфазные поверхностные натяжения практически не успевают измениться. Такое растекание можно рассматривать как неравновесное. [6]
Кинетический режим - режим протекания процесса, когда его скорость всецело определяется скоростью химической реакции. [7]
Кинетический режим - единственный режим, для которого скорость абсорбции пропорциональна задержке жидкости. [8]
Кинетический режим разрушения - режим поверхностного разрушения теплозащитных покрытий, подвергнутых конвективному или радиационному тепловому воздействию, скорость которого в основном определяется кинетикой реакции взаимодействия вещества покрытия и химически активных компонент набегающего газового потока. Характерной чертой этого режима разрушения является сильная ( экспоненциальная) зависимость скорости уноса массы от температуры ( см. гл. В отличие от режима сублимации скорость разрушения здесь существенно зависит от содержания в потоке химически активных компонент. Частным случаем кинетического режима, когда реакция имеет нулевой порядок, может считаться деструкция полимеров ( см. гл. [9]
 |
Схема двухмерного. [10] |
Кинетический режим роста частиц характерен при кристаллизации. Дело в том, что присоединение атомов ( молекул, ионов - в зависимости от типа решетки растущего кристалла) к идеальной плоской поверхности кристаллика связано с возникновением дополнительных затруднений, сходных с теми, которые имеют место при образовании самих зародышей новой фазы, когда подошедшие молекулы на поверхности кристаллика группируются в виде новой кристаллической плоскости. [11]
Различие кинетических режимов объясняется различным характером диссипации энергии для длинных и коротких волн. [12]
Изменения кинетического режима будем относить к смешанному типу, если они обусловлены одновременными изменениями режимов первого и второго рода. Этот случай весьма характерен для реакций, протекающих без образования защитного слоя твердого продукта: достаточно большие изменения значений действующих факторов могут привести одновременно к смене определяющей стадии и изменению отношения масштабов времени для процессов образования и роста зародышей. [13]
В кинетическом режиме определяющей стадией процесса является реакция, вызванная максимальной движущей силой. [14]
В кинетическом режиме k не зависит от давления. В диффузионном К изменяется пропорционально коэффициенту диффузии D и, следовательно, обратно пропорционально давлению. [15]
Страницы: 1 2 3 4