Значение - эквивалентная электропроводность
Cтраница 2
В этом и последующих уравнениях значения эквивалентной электропроводности, вычисленные по уравнению ( 3), обозначаются через А в отличив от определяемых опытным путем зиачс - 0832 ний А. [16]
 |
Числа переноса катионов. [17] |
В этом и последующих уравнениях значения эквивалентной электропроводности, вычисленные по уравнению ( 3), обозначаются через А в отличие от определяемых опытным путем значений А. [18]
Хотя ионные электропроводности могут быть получены из значений эквивалентной электропроводности ряда электролитов путем сравнения этих значений, однако гораздо более совершенным является метод их вычисления с помощью точных величин чисел переноса; числа переноса определяются относительными скоростями ионов, присутствующих в растворе, и, следовательно, связаны с относительными ионными электро-проводностями. Методика измерения чисел переноса, а также метод вычисления ионных электропроводностей будут описаны в гл. В столбцах под заголовком ос приведены приближенные величины температурных коэффициентов; их значение будет разъяснено на стр. [19]
Предварительные исследования смесей, показавшие, что изменения значений эквивалентной электропроводности при разведении могут быть с достаточным приближением вычислены суммированием изменений эквивалентной электропроводности для электролитов, составляющих смесь, дают основание перейти к природным водам. [20]
При этом использована разница в равновесных концентрациях ионов и значения эквивалентной электропроводности ионов при определенной ионной силе раствора. [22]
В то же время основной причиной огромных расхождений между значениями эквивалентной электропроводности сильных и слабых электролитов при конечных разведениях приходится считать в первую очередь различное число ионов в этих растворах. [23]
Для нескольких водных растворов 1 - 1 электролитов, имеющих общий катион, известны значения эквивалентной электропроводности К при различных напряженностях электрического поля V и определенной концентрации с. [24]
Для нескольких водных растворов 1 - 1 электролитов, имеющих общий катион, известны значения эквивалентной электропроводности А, при различных напряженностях электрического поля Ч и определенной концентрации с. [25]
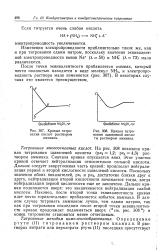 |
Кривые титрования кислот раствором аммиака.| Кривая титро вания щавелевой кислоты раствором аммиака. [26] |
Изменения электропроводности приблизительно такие же, как и при титровании едким натром, поскольку значения эквивалентной электропроводности ионов Na ( Я 50) и NHl ( A, 73) мало различаются. [27]
Второй вопрос, возникающий при вычислении электропроводности раствора смесей электролитов-для какой концентрации следует принимать значение эквивалентной электропроводности раствора отдельного электролита - для той, в которой он присутствует в данной смеси, или же для концентрации, равной суммарной концентрации смеси. [28]
Откладывая на оси абсцисс вместо с корень квадратный из концентрации, а по оси ординат значение эквивалентной электропроводности, получим уравнение прямой. [29]
В данном уравнении искомыми величинами являются общая концентрация солей в воде, концентрация сульфатов и значения эквивалентной электропроводности для хлоридов, гидрокар бонатов и сульфатов, зависящие от общей концентрации солей. Одни величины определяют другие и в то же время все они являются неизвестными. Однако, несмотря на это, имеется возможность получить ориентировочные представления о количестве солей в воде, а следовательно, и о значениях эквивалентной электропроводности для хлоридов, бикарбонатов и сульфатов и о количестве сульфатов. [30]
Страницы: 1 2 3 4
