Значение - эквивалентная электропроводность
Cтраница 3
Вероятно, авторы не избрали такой путь расчета в связи с тем, что встретили затруднение в подборе значений эквивалентной электропроводности отдельных электролитов. [31]
Если применяют щелочь другой концентрации, то знаменатель уравнений ( 19), ( 21) и ( 22) изменяется; значения эквивалентной электропроводности растворов NaOH различной концентрации и температурные коэффициенты этих величин берут из справочников. [32]
В настоящее время в литературе уже редко встречаются работы по изысканию общих переводных коэффициентов для всех типов вод, так как слишком очевидно различие значений эквивалентной электропроводности разных солей и непропорциональность их изменений с изменением концентраций. [33]
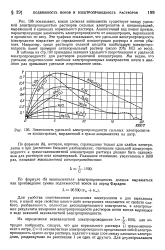 |
Зависимость удельной электропроводности сильных электролитов от концентрации, выраженной в грамм-эквивалентах на литр. [34] |
Для удобства сопоставления различных электролитов и для выявления того, в какой мере свойства какого-либо электролита отличаются от свойств слабого, разбавленного, полностью диссоциированного электролита, в электрохимии результаты измерения электропроводности растворов почти всегда выражают в виде значений эквивалентной электропроводности. [35]
При 18 С абсолютные скорости катиона и аниона валериановой кислоты ( С6НПСООН) соответственно равны 3 242 - 0 - 3см2 / сек-в и 2 662 - Ю - см / сек-в при напряжении поля, равном 1 в / см. Найти значение эквивалентной электропроводности валериановой кислоты при бесконечном разбавлении. [36]
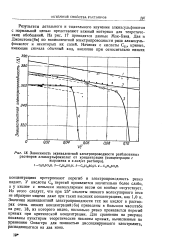 |
Зависимость эквивалентной электропроводности разбавленных. [37] |
У кислоты Сэ перегиб проявляется значительно более слабо, а у кислот с меньшим молекулярным весом он вообще отсутствует. Значения эквивалентной электропроводности тех же кислот в растворах очень низких концентраций [ 6в ] приведены в большом масштабе на рис. 18, из которого видно, насколько резко проявляется перегиб кривых при критической концентрации. Для сравнения на рисунке показаны пунктиром теоретические наклоны кривых, вычисленные по уравнению Онзагера для полностью диссоциирующего электролита, распадающегося на два иона. [38]
Расчет электропроводности следует производить по электропроводностям солей ( гипотетических), полученных сочетанием ионов. Для расчета следует принимать значение эквивалентной электропроводности каждой соли, входящей в раствор, при концентрации, равной общей концентрации смеси. [39]
XX XlOOO v, где - л - удельная электропроводность, то - концентрация в молях на 1 см3, v - объем в литрах, в [ котором содержится 1 моль электролита. Нередко вместо молярной электропроводности [ г приводят значения эквивалентной электропроводности А. Часто электропроводность относят не к числу молей или грамм-эквивалентов в литре, а к числу молей или граммэквивалентов в 1000 г растворителя. Применение такой концентрации имеет то преимущество, что она не зависит от температуры. [40]
Как следует из работы [3], малая зависимость емкости от концентрации электролита при больших отрицательных зарядах может быть связана также с тем, что большая часть соли в органическом растворителе находится в недиссоциированном состоянии. Для выяснения этого вопроса нами были определены значения эквивалентной электропроводности А, и вязкости т ] для растворов LiNO3 в ФА и ДМФ. Полученные данные приведены в таблице. Из таблицы видно, что хотя с ростом концентрации LiNO3 от О IN до насыщенного раствора величина Я падает на 1 - 2 порядка, но в основном этот эффект обусловлен не уменьшением степени диссоциации, а соответствующим увеличением вязкости раствора. [41]
Расчетные данные, полученные по формулам 2 и 3, хорошо согласуются с данными измерений. Таким образом, при расчете эквивалентной электропроводности раствора смеси электролитов следует принимать значения эквивалентной электропроводности для отдельного электролита при концентрации, равной общей концентрации смеси, а не при концентрации данного электролита в смеси. [42]
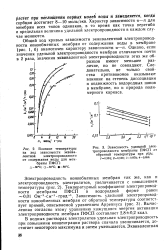
Общий ход кривых зависимости эквивалентной электропроводности ионообменных мембран от содержания воды в мембране ( рис. 1, б) аналогичен характеру зависимости к-п. Однако, если значения удельной электропроводности мембран отличаются почти в 2 раза, значения эквивалентной электропроводности этих же образцов имеют меньшее различие, но не совпадают. Следовательно, не только свойства противоионов оказывают влияние на степень диссоциации и подвижность водородных ионов в мембране, но и природа полимерного каркаса. [44]
Для выяснения возможности использования различий в изменениях эквивалентной электропроводности при разведении проведены предварительные исследования смесей электролитов. Эти исследования показали, что у разбавленных растворов смесей электролитов с общими ионами изменение значений эквивалентной электропроводности при разведении весьма близко к сумме изменений эквивалентных электропроводно-стей отдельных солей, составляющих данную смесь. [45]
Страницы: 1 2 3 4