Значение - эквивалентная электропроводность
Cтраница 4
Другой величиной, необходимой для вычисления удельной электропроводности раствора, является эквивалентная электропроводность ионов. При использовании в расчетах полных уравнений кривых титрования в каждый взятый для расчета момент титрования можно определить значение эквивалентной электропроводности ионов при данных условиях. Таким образом, может быть вычислена удельная электропроводность раствора при титровании. [46]
Найденный метод определения общей минерализации природных вод по электропроводности и содержанию гидрокарбонатов и хлоридов основан на учете зависимости электропроводности от общей концентрации, состава и процентного соотношения солей в исследуемой воде способом последовательных приближений. Этот учет оказалось возможным осуществить после того, как было показано, что эквивалентная электропроводность растворов смесей электролитов может быть вычислена с достаточным приближением по значениям эквивалентной электропроводности растворов отдельных электролитов, составляющих эту смесь, если эти значения эквивалентной электропроводности для каждого электролита взяты при общей концентрации смеси, а не при концентрации данного электролита. Расчет по этому методу ведется не по ионному составу, а по предполагаемому солевому составу, найденному по изложенному в работе способу. [47]
Найденный метод определения общей минерализации природных вод по электропроводности и содержанию гидрокарбонатов и хлоридов основан на учете зависимости электропроводности от общей концентрации, состава и процентного соотношения солей в исследуемой воде способом последовательных приближений. Этот учет оказалось возможным осуществить после того, как было показано, что эквивалентная электропроводность растворов смесей электролитов может быть вычислена с достаточным приближением по значениям эквивалентной электропроводности растворов отдельных электролитов, составляющих эту смесь, если эти значения эквивалентной электропроводности для каждого электролита взяты при общей концентрации смеси, а не при концентрации данного электролита. Расчет по этому методу ведется не по ионному составу, а по предполагаемому солевому составу, найденному по изложенному в работе способу. [48]
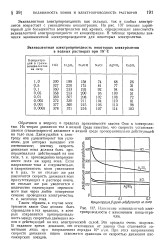 |
Изменение эквивалентной электропроводности с изменением концентрации. [49] |
Эквивалентная электропроводность как сильных, так и слабых электролитов возрастает с уменьшением концентрации. На рис. 137 показан характерный для большинства электролитов вид кривых, определяющих зависимость эквивалентной электропроводности от концентрации. В таблице приведены значения эквивалентной электропроводности для некоторых электролитов. [50]
Обычно вычисление ионной силы воды производится по данным химического анализа. В основу исследования было положено различие в изменениях значений эквивалентной электропроводности растворов различных солей с разведением. Как уже было указано выше, у растворов двух-двухвалент-ных электролитов эти изменения значительно больше, чем у растворов одно-одновалентных электролитов. [51]
В данном уравнении искомыми величинами являются общая концентрация солей в воде, концентрация сульфатов и значения эквивалентной электропроводности для хлоридов, гидрокар бонатов и сульфатов, зависящие от общей концентрации солей. Одни величины определяют другие и в то же время все они являются неизвестными. Однако, несмотря на это, имеется возможность получить ориентировочные представления о количестве солей в воде, а следовательно, и о значениях эквивалентной электропроводности для хлоридов, бикарбонатов и сульфатов и о количестве сульфатов. [52]
Другие производили измерение электропроводности вод в большом разведении, учитывая то обстоятельство, что значения эквивалентной электропроводности растворов различных электролитов по мере разведения несколько сближаются. [53]
Двукратное измерение электропроводности воды ( неразведенной и разведенной в 2 раза) дает возможность определять значение ионной силы воды. Определение ионной силы воды основано на неодинаковом изменении эквивалентной электропроводности различных солей при разведении. Наибольшее изменение при разведении показывают соли, составленные из двухза-рядных ионов, например CaSC4 и MgSO4, наименьшее - соли с однозарядными ионами, например Nad и КС1; соли, составленные из двухзарядных и однозарядных ионов, как, например, N32804 и Оа ( НСО3) 2, показывают изменения промежуточной величины. Так как отношение ионной силы раствора, содержащего однозарядные ионы, к числу г-экв / л этих ионов равно единице и в растворах, содержащих только двухзарядные ионы, равно двум, а изменение значений эквивалентной электропроводности растворов различных солей при разведении также зависит от соотношения двухвалентных и одновалентных ионов, то это свойство и было использовано для определения ионной силы раствора. [54]
 |
Понижение температуры замерзания NH3 при добавлении КВг. [55] |
При температурах ниже - 42 происходит расслаивание на две жидкие фазы - синюю и бронзовую. На рис. 38 показано изменение электропроводности растворов металлического натрия в жидком аммиаке в зависимости от концентрации. В разбавленных растворах электропроводность сходна с электропроводностью солей: молярная электропроводность имеет тот же порядок величины, как у раствора KNO3, и уменьшается при повышении концентрации. Предполагают, что в разбавленном растворе натрий диссоциирует на ион Na и сольватированный электрон. Концентрированные растворы имеют очень высокую элекропроводность, приближающуюся к значению эквивалентной электропроводности, равному 8 - Ю4 ом-г - см2 на 1 г-атом Na при насыщении. Это значение сравнимо со значением 5 - Ю6 ом - см2 на 1 г-атом твердого натрия. Такую высокую электропроводность нельзя объяснить миграцией ионов; она указывает на делокализа-цию электронных волновых функций, как в металлах. [56]
Страницы: 1 2 3 4