Значение - энергия - электрон
Cтраница 3
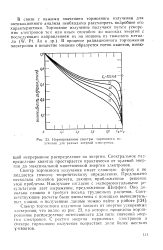 |
Нормированные спектры тормозного излучения для разных энергий электронов. [31] |
Спектр тормозного излучения зависит от энергии ускоренных электронов, что видно из рис. 23, на котором приведено нормированное распределение интенсивности для пяти значений энергии электронов. С ростом энергии первичных электронов в спектре тормозного излучения возрастает доля более жестких Y-КВЭНТОВ. [32]
Квантовый выход фотоэффекта для металлов при v v0 возрастает с увеличением v вплоть, до значений vi Wi I / ft, где Wt - значение энергии электрона на самом нижнем уровне зоны проводимости. При fa 2ЛМИН становится возможным явление каскадного фотоэффекта ( выбивания одним фотоном двух и более фотоэлектронов), вызывающее увеличение квантового выхода фотоэффекта. [33]
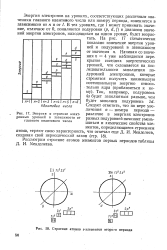 |
Энергия и строение электронных уровней в зависимости от главного квантового числа.| Строение атомов s - элементов второго периода. [34] |
В тех уровнях, где / может принимать значение, отличное от 0, появляются подуровни ( р, d, f) и диапазон значений энергии электронов, находящихся на одном уровне, будет возрастать. [35]
В тех уровнях, где / может принимать значение, отличное от 0, появляются подуровни ( р, d, f) и диапазон значений энергии электронов, находящихся на одном уровне, будет возрастать. [36]
Атомные остовы ( ионы металла) нарушают распространение волн де Бройля, аналогично интерференции рентгеновских лучей, проходящих через кристалл; для заданного направления распространения существуют запрещенные значения длин волн и соответственно запрещенные значения энергии электрона. [37]
 |
Зависимость энергии электрона от величины главного квантового числа ( а. линии водорода в видимой части спектра ( б. [38] |
Таким образом, теория строения водо-рбдного атома Бора открыла перспективы дальнейшего изучения строения атомов тем, что неоспоримо установила: 1) неприменимость законов классической физики к изучению атомных структур; 2) возможность ряда стабильных состояний атомов, при которых не происходит изменения энергии; 3) дискретность возбуждения атома за счет перескока электрона на более удаленные орбиты; 4) слоистость строения атома ( были определены значения энергий электрона каждого слоя); 5) дала объяснение и расчет спектров водородного атома. [39]
Таким образом, теория строения водородного атома Бора открыла перспективы дальнейшего изучения строения атомов тем, что неоспоримо установила: 1) неприменимость законов классической физики к изучению атомных структур; 2) возможность ряда стабильных состояний атомов, при которых не происходит изменения энергии; 3) дискретность возбуждения атома за счет перескока электрона на более удаленные орбиты; 4) слоистость строения атома ( были определены значения энергий электрона каждого слоя); 5) дала объяснение и расчет спектров водородного атома. [40]
В том случае, если существует несколько групп альфа-частиц, приведены значения энергий альфа-частиц, относящиеся к группе с наивысшей энергией и к тем группам, содержание которых превышает десять процентов. Значения энергий электронов конверсии приведены только в том случае, если неизвестно, в какой оболочке имеет место внутренняя конверсия или если не делалось попытки связать электроны с наблюденными или недоступными наблюдению гамма-лучами; во всех других случаях соответствующие данные приведены в столбце для гамма-лучей. [41]
Для оценки экранирования Слэтером было предложено несколько эмпирических правил [24], упрощающих и усредняющих распределение электронной плотности для различных орбиталей. Хотя значения энергии электронов, определенные по правилам Слэтера, не отличаются большой точностью, они позволяют выполнять простые расчеты и могут быть полезны при оценке таких относительных величин, как, например, кажущиеся размеры атомов и электроотрицательность элементов. [42]
Из значений энергий Ферми электронов в металлах следует, что их химический потенциал велик, а отсюда, согласно уравнению ( 15), велико также и Я. [43]
Каждому способу движения электрона отвечает определенное значение энергии. Каждому значению энергии электрона в атоме отвечает определенная атомная орбиталъ. Каждой атомной орби-тали отвечает определенная форма и размер электронного облака. [44]
Каждому способу движения электрона отвечает определенное значение энергии. Каждому значению энергии электрона в атоме отвечает определенная атомная орбиталь. Каждой атомной орби-тали отвечает определенная форма и размер электронного облака. [45]
Страницы: 1 2 3 4