Стереохимический результат
Cтраница 1
Стереохимические результаты в случае ацетонитрила, кето-нов и других изученных растворителей ближе к результатам, полученным в толуоле, чем в диоксане. Почти все эти растворители обладают более высокими диэлектрическими прони-цаемостями по сравнению с диоксаном и толуолом, и диссоциация ионных пар теперь уже больше не является чрезмерно трудной. [1]
Стереохимический результат этой реакции - рацемизацию в случае обоих диастереомерных бромидов - можно объяснить лишь в том случае, если допустить, что промежуточно образующиеся в стадии I свободные радикалы RR R C имеют плоскую конфигурацию. [2]
Стереохимические результаты завуалированы побочными процессами: рацемизацией и изомеризацией исходных ртутноорганиче-ских соединений, а также сольволизом, однако авторы полагают, что собственно протолиз протекает с полным сохранением конфигурации. [3]
Стереохимический результат классической 5 2-реакции - полная инверсия конфигурации (9.2.1), но, согласно определению Ингольда, стереохимическим результат 5V1 -реакции может быть любым: от полной рацемизации до полной инверсии. Любая реакция, идущая через полиостью диссоциированные ионы, должна привести к полной рацемизации. Частичная рацемизация характерна для реакций с участием сольватно-разделенных ионных пар. [4]
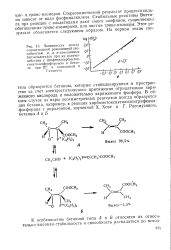
Стереохимический результат процесса сильно зависит от вида фосфиналкилена. Стабильные реактивы Витти-га при реакции с альдегидами дают смеси олефинов, существенно обогащенные транс-изомерами, или чистые транс-изомеры. Этот результат объясняется следующим образом. [6]
Стереохимический результат гидрирования во многих случаях существенно зависит от природы катализатора. Причины столь сильной зависимости не вполне ясны. По-видимому, приходится принять, что на палладиевом катализаторе значительно интенсифицируется превращение 1 2-диметилциклогексена в 2 3-изомер, десорбция и реадсорбция которого в процессе гидрирования и определяют, в конечном счете, стереохимию реакции. [7]
Стереохимические результаты разрыва связи О - ацил и О - алкил при гидролизе сложных офиров очень различны. [8]
Стереохимические результаты разрыва связи О - ацил и О - алкил при гидролизе сложных эфиров очень различны. [9]
Стереохимический результат восстановления кетонов мало зависит от характера и числа заместителей у атома олова. Вследствие большого эффективного объема восстановителя образуется меньше стабильных экваториальных изомеров, чем при восстановлении алюмогидридом лития. [10]
Стереохимический результат мономолекулярного нуклеофильного замещения может быть различным. [11]
Стереохимическим результатом должно быть сохранение конфигурации при атоме углерода. [12]
Нормальным стереохимическим результатом нуклеофильных бимолекулярных замещений ( SN2) является обращение конфигурации, потому что, вследствие большей отталкивающей силы и большей плотности электронов, переходное пирамидальное состояние I ( сохранение конфигурации) обладает более высокой энергией, чем линейное переходное состояние II ( обращение конфигурации), при котором этот эффект значительно снижен. [13]
Определите стереохимический результат ( сохранение или обращение) в каждой из приведенных ниже реакций, де С10Н7 представляет собой 1-нафтил ( см. также 1, стр. [14]
Этот стереохимический результат объясняется механизмом гидрирования на твердой поверхности; адсорбция молекулы арена на поверхности катализатора обеспечивает цис-ориентацию метальных групп в продукте реакции. [15]
Страницы: 1 2 3 4