Стереохимический результат - реакция
Cтраница 3
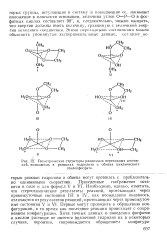 |
Геометрические структуры различных переходных состояний, возможных в реакциях гидролиза и обмена циклического. [31] |
Приведенные соображения остаются в силе и для формул V и VI. Необходимо, однако, отметить, что стереохимические результаты реакций, протекающих через промежуточные состояния III и IV, как неожиданно оказалось, отличаются от результатов реакций, протекающих через промежуточные состояния V и VI. Первые могут проводить к обращению конфигурации, в то время как последние реакции происходят с сохранением конфигурации. [32]
Как можно предположить, исходя из рассмотрения механизмов, реакции раскрытия цикла в щелочных или нейтральных условиях приводят к обращению конфигурации у атома углерода, подвергшегося атаке; это справедливо также и для многих реакций, катализируемых кислотами. Однако растворитель также может играть важную роль в определении стереохимического результата реакции. Обработка ( - т -) - ( К) - 2-фенилоксирана хлоридом водорода в хлороформе дает [66] 2-фенил - 2-хлорэтанол с преимущественным обращением при С-2, тогда как реакция в сухих эфирах приводит к 2-фенил - 2-хлорпроизводному, где конфигурация при С-2 в основном сохранена. В последнем случае, в качестве интермедиата, по-видимому, выступает сольватированная ионная пара. [33]
Как можно предположить, исходя из рассмотрения механизмов, реакции раскрытия цикла в щелочных или нейтральных условиях приводят к обращению конфигурации у атома углерода, подвергшегося атаке; это справедливо также и для многих реакций, катализируемых кислотами. Однако растворитель также может играть важную роль в определении стереохимического результата реакции. Обработка () - ( Рч) - 2-фенилоксирана хлоридом водорода в хлороформе дает [66] 2-фенил - 2-хлорэтанол с преимущественным обращением при С-2, тогда как реакция в сухих эфирах приводит к 2-феннл - 2-хлорпронзводному, где конфигурация при С-2 в основном сохранена. В последнем случае, в качестве интермедиата, по-видимому, выступает сольватнрованная ионная пара. [34]
Атака бромид-ионом идет преимущественно со стороны, противоположной брому в этом ионе, что и определяет стереохимический результат реакции как яняш-присоединение. [35]
Внедрение дихлоркарбена, генерируемого в условиях межфазного катализа, происходит с сохранением стереохимической конфигурации. Отметим, что, возможно, в реакции промежуточно образуется контактная ионная пара, изображенная ниже, но не свободный карбониевый ион, поскольку стереохимическим результатом реакции является сохранение конфигурации. [36]
Пятихлористый фосфор ( РС15) эффективен как при замещении ОН - С1 при первичном и вторичном атоме углерода, так и при превращении С - С0 - группировки в С - СС12 - или ССС1 - группировку. Промышленный РС15 содержит в качестве примесей Fe, HC1, FeCl3, PC13, POC13, которые очень сильно влияют на реакционную способность РС18 и могут совершенно изменить стереохимический результат реакции. [37]
Если уходящая группа может служить донором протонов, то конфигурация сохраняется даже при отсутствии в реакционной среде иных источников протонов. Однако если в среде имеются другие доноры протонов, то в роли электрофильных агентов выступают именно они. В случае когда с атомом углерода, при котором происходит замещение, связаны протонодонорные группировки, стереохимический результат реакции будет зависеть от числа доступных протонов и их ориентации. [38]
Следовательно, отщепление галогеноводорода в этих условиях должно происходить в основном как ыс-элиминирование. Весьма вероятно также, что газофазная реакция должна быть более похожа на жидкофазную реакцию в неполярном растворителе, чем на аналогичную реакцию в полярном растворителе. В силу этих доводов ыс-направленность газофазного элиминирования более уже не кажется аномальной. Стереохимические результаты реакции присоединения интерпретируются в терминах устойчивости ионных пар, образованных карбониевыми ионами и анионами. [39]
Полученный силанол имел оптическую чистоту только 50 %, что соответствует 75 % - ному обращению конфигурации. Очевидно, что любая атака основанием карбонильного атома углерода должна была бы вести к силанолу без обращения конфигурации. Неполная оптическая чистота выделенного продукта может объясняться либо частичной реакцией по карбонильной группе, либо недостаточной стереоспецифичностью реакции, или и тем и другим вместе. Во всяком случае, преобладающим стереохимическим результатом реакции является обращение конфигурации и атака поэтому кремния протекает быстрее, чем атака по атому углерода карбонильной группы. [40]
Это превращение называется реакцией Виттиг а. Для отщепления галогеноводорода используют различные основания ( в вависимостя от характера алкяльной группы): алкоголяты натрия, амид натрия, димсил-нагрий или алкиллитий. Первая стадия реакции проводится в растворе бензола иди нитрометана, вторая - реакция отщепления - требует более основного растворителя, такого, как эфир или ТГФ. Что касается последней стадии - взаимодействия с карбонильным соединением, то выбор растворителя ока-вывает определенное влияние на стереохимический результат реакций, как будет видно из дальнейшего, и поэтому далеко не безразличен. [41]
В частности, известны примеры стереоспецифичного протекания реакции получения хлоргидринов. Об этом говорит, например, факт получения трянс-2 - хлорциклогексанола с выходом 75 % при взаимодействии цикло-гексена с хлором в водном растворе гидроксида натрия. Цикл иона раскрывается за счет атаки гидроксид-ионом ( или молекулой воды) с тыльной стороны, так что стереохимическим результатом реакции оказывается амтм-диаксиальное присоединение. Конечно, образовавшийся ( а а) - хлор-гидрин сразу же принимает ( е е) - конформацию. [42]
Используя это принцип, Бенджамин, Шеф-фер и Коллинз [114] с помощью двухстадийного гриньяровского синтеза с фенилмагнийбромидом получили из каждого энантиомера аланина дифенил-карбиноламин Мак-Кензи, Роджера и Уилса ( стр. В обоих случаях подтвердились данные Мак-Кензи, Роджера и Уилса, согласно которым при дезаминировании миграция фенильной группы происходит на 88 % с обращением и на 12 % с сохранением конфигурации у конечного места миграции. Затем инвертированный продукт был отделен от рацемического продукта и путем расщепления было установлено положение радиоактивной метки. Во-первых, согласно общей электронной схеме, развитой и описанной в разд. X и присоединения R к конечному месту миграции В является нуклеофильным замещением, поскольку и входящая и уходящая группы перемещаются вместе со своими электронами связи. Если изменение связей происходит достаточно синхронно и поэтому локальный процесс носит характер S - замещения ( хотя общий процесс замещения относится к SNl-THny), то стереохимическим результатом реакции должна быть инверсия конфигурации у конечного места миграции. X ( в данном случае NJ) происходит без участия постороннего нуклео-фила. Кроме того, необходимо вспомнить тот вывод, который был сделан в разд. [43]
Страницы: 1 2 3