Атомный вес - водород
Cтраница 3
В 1815 и 1816 гг. в Анналах философии появились две анонимные статьи54, в которых, в частности, была высказана идея, что атомные веса всех элементов ( и следовательно, соединений - сложных атомов) являются кратными атомному весу водорода, принятому за единицу. Издатель журнала Томсон с энтузиазмом встретил новую идею и в одной из статей, опубликованных в 1816 г., сообщил, что автором идеи является доктор У. [31]
Можно ли округлять атомный вес водорода с 1 0080 до 1 01 в расчете анализа, проводимого с допустимой ошибкой в 0 1 %, если: а) в расчетной формуле атомный вес водорода является множителем; б) атомный вес водорода входит в молекулярный вес H2SO4, который и является множителем. [32]
Задолго до Ричардса, в 1895 г., американский ученый Морли установил, что весовое отношение водорода к кислороду в воде равно 1 8467 г: 14 656 г. Пользуясь современной шкалой атомных весов, попытаемся вычислить на основании этих данных атомный вес водорода. [33]
В этих и других соединениях водорода минимальный вес водорода в стандартном объеме газа, как установлено, равен 1 г, и вес его во всех случаях является кратным этому минимальному весу, следовательно, это значение можно принять в качестве атомного веса водорода. Из табл. 20 видно, что водород состоит из двухатомных молекул Н2, а вода имеет формулу ( Н20) ж, причем х следует определить. [34]
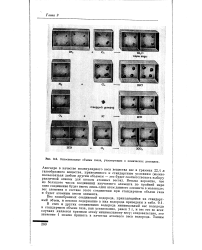 |
Относительные объемы газов, участвующих в химических реакциях. [35] |
В этих и других соединениях водорода минимальный вес водорода в стандартном объеме газа, как установлено, равен 1 г, и вес его во всех случаях является кратным этому минимальному весу; следовательно, это значение 1 можно принять в качестве атомного веса водорода. [36]
Если недоверие к системе атомных весов Берцелиуса связано главным образом с усилившимся недоверием к ее объемной основе, то недоверие к системе атомных весов английских химиков, и в частности Томсона, объясняется тем, что Томсон, убежденный в правильности гипотезы Праута о кратности атомных весов элементов атомному весу водорода, произвольно округлял атомные веса тех элементов, которые выражались дробными числами, оправдывая это не только теоретическими соображениями, но также и тем, что в таком виде легче запомнить значение этих атомных весов. [37]
Рассмотрим критику Менделеевым принципа аддитивности в отношении: а) удельных объемов химических соединений ( молекул), б) атомных весов химических элементов ( атомов) и затем остановимся на том, как истолковывал Менделеев свой периодический закон в связи с неаддитивностью атомных весов по отношению к атомному весу водорода. [38]
Атомный вес водорода обозначим через А. Возьмем другой элемент с атомным весо. [39]
Потому что эквивалентный вес водорода равен единице, не правда ли. Атомный вес водорода равен единице и валентность его тоже единица. [40]
Химическая формула вещества показывает не только его состав, но и весовое соотношение составляющих вещество элементов. Например, атомный вес водорода равен 1 008, а кислорода 16, следовательно, в воде Н2О на 2 016 весовой части водорода приходится 16 весовых частей кислорода. [41]
Эквивалентный вес водорода равен его атомному весу. Так как атомный вес водорода равен 1 008, то этому же числу равен и его эквивалентный вес. [42]
Смешение понятий вело и к серьезной ошибке в истолковании теории Авогадро. Неудачный выбор единицы молекулярных весов ( атомный вес водорода 0 5) также препятствовал быстрому признанию закона Авогадро. [43]
Приняв атомный вес углерода равным 12 01115, рассчитайте атомный вес водорода. [44]
Когда измерили атомные веса, то они оказались совсем не кратными атомному весу водорода, и идея была на время отвергнута. [45]
Страницы: 1 2 3 4