Атомные весы
Cтраница 1
Таблица атомных весов ежегодно - исправляется особой международной комиссией. [1]
Таблица атомных весов ежегодно исправляется особой международной комиссией. [2]
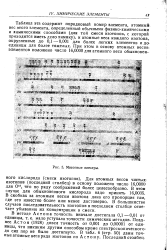 |
Массовые спектры. [3] |
Для атомных весов чистых: изотопов ( последний столбец) в основу положено число 16 0000 для О16, что по ряду соображений более целесообразно. В скобках за атомным весом изотопа дана его пропорция там, где это известно более или менее достоверно. В большинстве случаев последовательность изотопов в последнем столбце отвечает убыванию их концентрации в смеси. [4]
Определение атомных весов производится с макроскопическими количествами вещества при посредстве химических анализов. Получаемые таким путем числа имеют огромное практическое значение и лежат в основе всех химических расчетов. Если предположить, как это и делалось до сравнительно недавнего времени, что все атомы данного элемента имеют одинаковую массу, то, пользуясь законом Авогадро, согласно которому в одном моле любого вещества содержится одно и то же количество молекул, можно при помощи химического атомного веса вычислить и абсолютную массу атома. [5]
Сопоставление атомных весов с весом водорода - утверждает Берцелиус 4 - не только не представляет никакого преимущества, но вызывает большие трудности, потому что водород очень легок и с трудом дает неорганические соединения. Наоборот, кислород имеет все преимущества. [6]
Система атомных весов, созданная огромными усилиями Берцелиуса, была далеко не удовлетворительна, и поэтому химики скоро почувствовали большую потребность в единой теории, лишенной противоречий и способной объяснить многочисленные фактические данные. [7]
Определение атомных весов этим способом приближается по точности к лучшим масспектрографическим измерениям. [8]
Из атомных весов находим: t M Mn Л / - 2Л / Не - 7 01822 1 00812 - 2 - 4 00390 0 01853 од. [9]
Системы атомных весов, принятые Вюрцем, Мейером, Одлингом и Лавровым, как мы видели, содержали ошибочные атомные веса некоторых элементов. [10]
Постоянства атомных весов все же недостаточно для объяснения того, что химические свойства элемента хотя и являются в действительности периодической функцией заряда ядра, все же могут быть представлены как периодическая функция атомного веса. Здесь важно то обстоятельство, что атомные веса элементов в общем возрастают в том же направлении, что и заряды ядер ( см. стр. Вследствие этого одинаковый порядок расположения элементов, за некоторым исключением, получают как в случае распределения их по возрастанию атомного веса, так и по возрастанию заряда. Заряды ядер непрерывно возрастают от 1 до 103 - наивысшего из установленных в настоящее время зарядов. Вместе с тем заряд ядра определяет положение каждого элемента в периодической системе. Пока не были известны заряды ядер и элементы располагали в порядке возрастания атомного веса, последнее обстоятельство не всегда выполнялось. Это происходило потому, что атомные веса изменяются не через равные интервалы. Вследствие этого на основании атомных весов нельзя было с достоверностью решить вопрос, должен ли между двумя известными элементами находиться еще один неизвестный элемент. В настоящее время установлено, что вплоть до элемента с зарядом ядра 103 ряд элементов является непрерывным. [11]
Постоянства атомных весов все же недостаточно для объяснения того, что химические свойства элемента хотя и являются в действительности периодической функцией заряда ядра, все же могут быть представлены как периодическая функция атомного веса. Здесь важно то обстоятельство, что атомные веса элементов в общем возрастают в том же направлении, что и заряды ядер ( см. стр. Вследствие этого одинаковый порядок расположения элементов, за некоторым исключением, получают как в случае распределения их по возрастанию атомного веса, так и по возрастанию заряда. Заряды ядер непрерывно возрастают от 1 до 103 - наивысшего из установленных в настоящее время зарядов. Вместе с тем заряд ядра определяет положение каждого элемента в периодической системе. Пока не были известны заряды ядер и элементы располагали в порядке возрастания атомного веса, последнее обстоятельство не всегда выполнялось. Это происходило потому, что атомные веса изменяются не через равные интервалы. Вследствие этого на основании атомных весов нельзя было с достоверностью решить вопрос, должен ли между двумя известными элементами находиться еще один неизвестный элемент. В настоящее время установлено, что вплоть до элемента с зарядом ядра 103 ряд элементов является непрерывным. [12]
Постоянства атомных весов все же недостаточно для объяснения того, что химические свойства элемента, хотя и являются в действительности периодической функцией заряда ядра, все же могут быть представлены как периодическая функция атомного веса. Здесь важно то обстоятельство, что атомные веса элементов в общем возрастают в том же направлении, что и заряды ядер ( см. стр. Вследствие этого одинаковый порядок расположения элементов, за некоторым исключением, получают как в случае распределения их по возрастанию атомного веса, так и по возрастанию заряда. Заряды ядер непрерывно возрастают от 1 до 104 - наивысшего из установленных в настоящее время зарядов. Вместе с тем заряд ядра определяет положение каждого элемента в периодической системе. Пока не были известны заряды ядер и элементы располагали в порядке возрастания атомного веса, последнее обстоятельство не всегда выполнялось. Это происходило потому, что атомные веса изменяются не через равные интервалы. Вследствие этого на основании атомных весов нельзя было с достоверностью решить вопрос, должен ли между двумя известными элементами находиться еще один неизвестный элемент. В настоящее время установлено, что вплоть до элемента с зарядом ядра 104 ряд элементов является непрерывным. [13]
Система атомных весов и формул химических соединений, предложенная шведским химиком, была самой совершенной в первой половине XIX в. Атомные веса Берцелиуса с незначительными исправлениями Реньо очень близки к современным, а формулы большинства химических со-одияений совпадают с современными. Этот выдающийся результат был достигнут Берцелиусом не только благодаря собственным чрезвычайно точным для того времени экспериментам, но и умению правильно оценить результаты, полученные его современниками. При этом необходимо учитывать, что в первой половине XIX в. До этого открытия химики фактически блуждали впотьмах, так как не было большой надежности в правильности того или иного атомного веса или формулы. [14]
Значения атомных весов даются округленные. [15]
Страницы: 1 2 3 4