Диметилэтинилкарбинол
Cтраница 2
Увеличение количества алифатического спирта или внесение в реакционную смесь диметилэтинилкарбинола тормозит реакцию. [17]
Таким образом, то или иное решение проблемы выделения диметилэтинилкарбинола определяется в конечном итоге требованиями к чистоте продукта и путями его дальнейшего использования. [18]
Фенилпропиоловая и коричная кислоты полярографировались на соответствующих фонах, а диметилэтинилкарбинол определялся с применением концентрированного раствора серебра. [19]
Активность разбавленных слоев палладий-иридиевых адсорбционных катализаторов в реакциях жкдко-фазного гидрирования диметилэтинилкарбинола / / Физ. [20]
С тех же позиций в лаборатории Д. В. Сокольского была исследована гидрогенизация диметилэтинилкарбинола на скелетном никеле в щелочном растворе. [21]
В первоначальном варианте ( рис. 33) установка была предназначена для получения диметилэтинилкарбинола в присутствии водного раствора едкого кали. После загрузки реагентов смесь охлаждают до температуры - 20 С и насыщают ацетиленом из баллона под давлением не выше 0 4 ати. Количество поданного в систему ацетилена контролируют по ротаметру 4 и по изменению веса баллонов. Избыток газов периодически сбрасывают из сатуратора 5 через обратный холодильник 1 и воздушку в атмосферу. [22]
С целью установления интервалов варьирования основных параметров при последующей оптимизации режима получения диметилэтинилкарбинола в проточной системе было исследовано влияние количества анионита, молярного соотношения реагентов и температуры на протекание процесса этинилирования ацетона в статических условиях в пробирочных автоклавах при полном смачивании смолы реакционной смесью. Молярное соотношение кетон: аннонит изменяли от 1: 1 до 1: 4, разбавляя смолу Si02 такого же зернения или разбавляя кетон диэтиловым эфиром. [23]
После нейтрализации щелочного катализатора и, отгонки аммиака ( его сжижают и возвращают в цикл) диметилэтинилкарбинол отделяют от непревращенного ацетона и направляют на следующие стадии процесса. Сообщается о высоком выходе изопрена, достигающем 90 %, но использование довольно дорогого сырья все равно делает этот метод малоперспективным. [24]
Для уточнения кинетической модели реакции этинилирования было детально изучено влияние различных факторов на степень превращения ацетона в диметилэтинилкарбинол. [25]
Наиболее распространенным способом проведения реакции этинилирования является предложенный еще в начале века А. Е. Фаворским [33] на примере получения диметилэтинилкарбинола вариант синтеза при атмосферном давлении в среде безводных органических растворителей в присутствии более чем эквимолекулярного количества едкого кали. Синтез дегидролиналоола реализован в нашей стране на пилотной установке Калужского комбината синтетических душистых веществ. Производство ацетиленовых спиртов С15 и С20 в несколько модифицированных условиях реакции Фаворского в промышленном масштабе освоено на Болохов-ском химическом комбинате и на Ереванском витаминном заводе. [26]
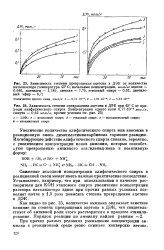
Было исследовано промотирование никеля на окиси алюминия ( 2 % Ni) платиной, палладием и родием при гидрировании диметилэтинилкарбинола в водно-спиртовом фосфатном буфере. Как видно из рисунка, скорость гидрирования двойной и тройной связей проходит через максимумы в случае, когда наносится 3 2 10-а г Pt, что соответствует примерно 1 атому Pt на 20 атомов Ni. При промотировании палладием и родием максимальные скорости достигаются при нанесении почти в 10 раз меньшего количества промотора ( в 5 раз меньше, в ат. [27]
В соответствии с этой схемой ацетон при конденсации с ацетиленом по методу Фаворского-Назарова легко и с высоким выходом превращается в диметилэтинилкарбинол; последний при гидрировании дает почти с количественным выходом простейший терпеновый спирт - диметилвинилкарбинсл. [28]
Синтез осуществлен путем конденсации диметилэтинилкарбинола, полученного конденсацией ацетона с ацетиленом по Фаворскому [2] с диметилаце-тилкарбинолом, который получался гидратацией диметилэтинилкарбинола по реакции Кучерова. [29]
Значительно позже, уже в 1933 г., А. Е. Фаворский [3] вновь возвратился к изучению реакции ацетиленового синтеза и разработал способ синтеза диметилэтинилкарбинола и ряда других этинилкарбинолов, основанный на конденсации ацетилена с ацетоном и другими различными кетонами в эфирном растворе в присутствии порошка едкого кали. В 1935 г. А. Е. Фаворский [4] предложил метод электрохимического восстановления этинилкарбинолов до винилкарбинолов, в результате чего была создана общая простая и удобная схема синтеза винилкарбинолов на основе ацетилена, в том числе и диметилвинилкарбинола, который А. Е. Фаворский [5] наряду с изобутенилкарбинолом считал простейшим терпеновым спиртом. [30]
Страницы: 1 2 3